19.06.2019
Kuinka tasapainottaa tärkeimmät hormonit ravinnon avulla. Hormonaaliset tasot syömishäiriöissä potilailla, joilla on metabolinen oireyhtymä Verikoe T4 kilpirauhashormonille: normit ja muutosten syyt
Kun hormonijärjestelmämme on tasapainossa, hormonit toimivat kehon viisaina mentoreina lähettäen "tee tämä" tai "tee niin" -komentoja kehomme soluille homeostaasin varmistamiseksi.
Homeostaasi on juuri se tila, jossa sinulla on upeat paksut hiukset, vahvat kynnet, kirkas iho, vakaa mieliala ja paino, olet stressinkestävä, sinulla on hyvä ruoansulatus ja libido.
Mutta valitettavasti hormonijärjestelmämme on jo hyvin herkkä ympäristövaikutuksille, erityisesti myrkkyjen vaikutukselle, huonolle unelle, aliravitsemukselle, suoliston mikroflooran epäjohdonmukaisuudelle ja jopa pahoille ajatuksille.
On 5 tärkeintä hormonia, jotka vaikuttavat kehon homeostaasiin, ja niiden tasapainottamiseksi ei tarvitse välittömästi turvautua lääkkeisiin tai ravintolisäisiin, vaan ensin on yritettävä säädellä tilannetta erityisesti valittujen lääkkeiden avulla. tuotteet, joilla on kyky palauttaa hormonaalinen tasapaino.
1. Korkea kortisoli
Kuinka hän toimii:
Kortisoli on tärkein stressireaktiohormoni, ja sitä tuottavat lisämunuaiset. Kohonnut kortisolitaso lisää verenpainetta ja sokeritasoa. Kroonisesti korkeat hormonipitoisuudet voivat johtaa lisääntyneeseen kiihottumiseen tai hankaluuteen kehossa, masennukseen, varhaiseen ikääntymiseen, painonnousuun, verensokeriongelmiin ja metaboliseen oireyhtymään.
Mitä saatat huomata:
- Tuntuu siltä, että olet jatkuvasti juoksemassa ja tekemässä tehtävää toisensa jälkeen.
- Vaikeudet painonpudotuksessa, erityisesti vyötärön ympärillä.
- Toistuvat mielialan vaihtelut tai masennus.
- Välittömän vihan tai raivon reaktion ilmentymä.
- Vaikeus rentoutua illalla ja huono uni.
- Heikot kynnet tai iho-ongelmat, kuten ekseema tai ohut iho.
- Korkea verenpaine tai korkea verensokeri (tai molemmat).
- Muistihäiriöt tai huomion puute, erityisesti stressin aikana.
- Suolaisen tai makean ruoan himo.
- Matala libido.
Ruokaratkaisu:
Ylimääräinen tumma suklaa voi alentaa kortisolihormonitasoja. Voit myös ajoittain käyttää luonnollisissa olosuhteissa kasvatettua kalaa. Herkullinen lääke, eikö?!
2. Liikaa testosteronia
Kuinka hän toimii:
Testosteroni on hormoni, jota tuotetaan naisten munasarjoissa, miesten kiveksissä ja lisämunuaisissa. Se on erittäin tärkeä hyvinvoinnin tunteen, itseluottamuksen, lihasten jäykkyyden ylläpitämisen, luuston kasvun ja seksuaalisen toiminnan kannalta. 30 % naisista kokee sen liiallisia määriä, mikä voi johtaa akneen, epäsäännöllisiin kuukautisiin, lisääntyneeseen kehon karvojen kasvuun, pään hiustenlähtöön ja hedelmättömyyteen.
Mitä saatat huomata:
- Akne.
- Ylimääräisiä hiuksia rinnassa, kasvoissa ja käsivarsissa.
- Rasvainen iho ja hiukset.
- Hiustenlähtö päässä (joskus yhdistettynä liialliseen kehon karvojen kasvuun).
- Kainalon värimuutos: Ne muuttuvat tummemmiksi ja paksummiksi kuin normaali ihosi.
- Papilloomat, erityisesti niskassa ja ylävartalossa.
- Hyperglykemia tai hypoglykemia tai epävakaa verensokeri.
- Lyhyt luonne tai ärtyneisyys, liian aggressiivinen autoritaarinen käytös.
- Masennus tai ahdistus.
- Munasarjojen monirakkulaoireyhtymä, johon liittyy tyypillisesti munasarjakystat, hedelmättömyys ja kuukautiskierto harvemmin kuin 35 päivän välein.
Ruokaratkaisu:
Syö enemmän vihreitä papuja sekä kurpitsan ja kurpitsan siemeniä, jotka kaikki sisältävät runsaasti sinkkiä, jolla on tärkeä rooli seksuaalisessa kehityksessä, kuukautisissa ja ovulaatiossa. Sinkin puute liittyy akneen ja kohonneisiin androgeenitasoihin, hormoniryhmään, johon testosteroni kuuluu.
Klikkaus " Kuten» ja saat parhaat julkaisut Facebookissa!
103. Indikaattorit, jotka kuvaavat kehon lipidiaineenvaihdunnan tilaa. Sisältö ja määritysmenetelmät verestä.
104. Monityydyttymättömät rasvahapot ovat tärkeitä ravitsemuksellisia tekijöitä. Polyeenihappojen rooli eikosanoidien lähteenä. Koulutus, biologinen rooli, prostaglandiinien ja leukotrieenien osallistuminen aineenvaihdunnan ja kehon toimintojen säätelyyn. Eikosanoidisynteesin estäjien tulehdusta ehkäisevä vaikutus.
105. Hiilihydraattien, rasvojen ja aminohappojen aineenvaihdunnan hormonaalinen säätely insuliinilla. Ruokavalion rytmin vaikutus hormonaaliseen tilaan.
106. biologinen hapetus. Energiamateriaalin yhdistämisen päävaiheet. Kataboliset prosessit ovat tärkeimmät vedyn luovuttajien lähteet hengitysketjussa. NADH:n intramitokondriaaliset ja ekstramitokondriaaliset lähteet.
107. Oksidatiiviset prosessit ovat NADH:n lähteitä. Sukkula entsyymi-substraattijärjestelmät vedyn siirtämiseksi mitokondrioihin. Prosessin arvo.
108. Katabolismin ja anabolismin käsite ja niiden suhde. Endergoniset ja eksergoniset reaktiot aineenvaihdunnassa. ATP ja muut korkean energian yhdisteet. ADP-ATP-sykli. Tärkeimmät reitit ADP:n fosforylaatioon ja ATP:n käyttöön. Kudosten hapen käyttötavat.
109. Oksidatiivisten prosessien loppuvaiheen ominaisuudet. Elektronien ja protonien kuljetusketjun rakenteellinen organisaatio. ATP - syntetaasi, ATP-synteesi. ATP on yleinen kemiallinen energian varastointimuoto soluun. Hapettumisen ja fosforylaation konjugaatiomekanismi. Mitchell-Skulachev-kemosmoottisen oksidatiivisen fosforylaation teorian karakterisointi.
110. Biologisen hapettumisen loppuvaihe. Hengitysketjun organisointi mitokondrioissa. Hapetuksen kytkeytyminen fosforylaatioon hengitysketjussa. H+-ATP-syntetaasi. Hengityksen hallinta. Hengityksen ja fosforylaation irtoaminen. Hypoenergeettiset tilat.
111. Soluhengityksen vaihtoehtoiset toiminnot: Mikrosomaalinen hapetus. Mikrosomaalisen elektroninkuljetusketjun tärkeimmät entsyymit. Tärkeimmät mekanismit endogeenisten ja vieraiden myrkyllisten aineiden neutraloimiseksi. Vieraiden aineiden muuntamisen ensimmäinen ja toinen vaihe.
112. Prooksidantti- ja antioksidanttiprosessit. Reaktiivisten happilajien muodostuminen. edustajat. Biomolekyylien ja rakenteiden vahingollisen vaikutuksen mekanismi. Antioksidanttinen puolustusjärjestelmä.
113. Antioksidanttijärjestelmän entsyymit. Katalaasi, rakenne, toiminnot. Entsymaattisen aktiivisuuden määrittäminen.
114. Veren fysiologiset toiminnot, osmoottinen ja onkoottinen paine. Proteiinit ja mineraalikomponentit veriplasman ylläpidossa.
115. Veren fysikaaliset ja kemialliset parametrit. pH:n pysyvyyden arvo organismin elämälle. Puskurijärjestelmät, esimerkkejä, biologinen rooli.
116. Käsite veren happo-emästilasta. Happo-emästasapainon rikkominen. Asidoosi ja alkaloosi, tyypit.
117. Veren plasman proteiinit. Luokittelu, sisältö, erottelumenetelmät. Yksittäisten murtolukujen ominaisuudet. biologinen rooli.
118. Veriplasman albumiini. biologinen rooli. Sisältö. Kvantitatiiviset määritysmenetelmät.
119. Veren entsyymit, luokittelu, lähteet, määrityksen diagnostinen arvo. Veren tärkeimmät indikaattorientsyymit.
120. Proteiinittomat typpeä sisältävät ja typettömät veren orgaaniset aineet. Sisältö, rooli elämänprosesseissa.
121. Nykyaikaiset käsitteet veren hyytymisjärjestelmästä. Plasma- ja verihiutaletekijät. rooli hemostaasissa.
122. Rullaava järjestelmä. Ulkoiset ja sisäiset hyytymisreitit. antikoagulanttijärjestelmä.
123. Mineraalit mikroravintoaineina. Lähteet ja tarve. Mineraalien yleiset toiminnot.
124. Natrium-, kalium-, kloori-ionien erityinen rooli kehon elämässä. Kalium, natrium, veren kloridit. Hypo- ja hypernatremia, hypo- ja hyperkalemia. Veren seerumin kloridien kvantitatiivinen määritys.
125. Kalsiumia, magnesiumia ja fosforia. Seerumin kalsiumin määritysmenetelmät, diagnostinen arvo. biologinen rooli. Kalsiumin ja fosforin aineenvaihdunnan säätely. Hormonihallinnan rooli ja mekanismi. D-vitamiinin osallisuus.
126. Rauta, lähteet, tarve, imeytyminen, kuljetusproteiinit, laskeuma, biologinen rooli.
127. Kupari. Biologinen rooli, määritysmenetelmät.
128. Hivenaineet: jodi, fluori, kupari, mangaani, erityiset toiminnot.
129. Vesi eksogeeninen ja endogeeninen, lähteet, tarve. Veden biologinen rooli. Veden, natriumin ja kaliumin vaihdon säätely kehossa.
130. Vesi-suola-aineenvaihdunnan säätely. Vasopressiinin ja aldosteronin rakenne, aineenvaihdunta ja vaikutusmekanismi. Reniini-angiotensiinijärjestelmä. Munuaisten hypertension kehittymisen biokemialliset mekanismit.
131. Hermoston biokemia. Energia-aineenvaihdunnan ominaisuudet. Hapen tarve. Hiilihydraattien aineenvaihdunta, lähteet. Glukoosin rooli aivojen substraatissa ja energiahuollossa.
132. Aivojen kemiallinen koostumus. Proteiinit, toiminnallinen luokitus. Hermokudoksen neurospesifiset proteiinit. Vapaiden aminohappojen rahasto. Dikarboksyylihappojen vaihdon ominaisuudet.
133. Aivojen lipidit ja hiilihydraatit: edustajat, biologinen rooli. Vaihteen ominaisuudet.
134. Neurotransmitterijärjestelmät, kriteerit. Kiihottavat ja estävät välittäjäaineet. Edustajat, ominaisuudet, koulutus ja inaktivointi.
135. Vapaiden aminohappojen rahasto aivoissa. Glutamiinihapon aineenvaihduntatavat. GABA:n muodostuminen, rooli aivoissa.
136. Biogeenisten amiinien rooli aivotoimintojen suorituskyvyssä. Katekolamiinit, indolamiinit, histamiini. Koulutus, erityiset toiminnot aivoissa, inaktivointi.
137. Hermokudoksen biologisesti aktiiviset peptidit. Rooli kivun ja anestesian havaitsemisessa, hermoston autonomisten ja korkeampien toimintojen säätelyssä.
138. Muistin biokemian käsite. Muistin tyypit, muodostumismekanismi.
139. Lihaskudoksen biokemia. Lihasproteiinit: myosiini, antini, aktomyosiini, tropomyosiini, troponiini. Sarkoplasmiset proteiinit.
140. Lihasten supistumisen ja rentoutumisen biokemialliset mekanismit. Säätelyproteiinien, kalsiumin rooli. Energiansyöttömekanismit.
141. Proteiinittomat typpipitoiset uuttoaineet, typpittömät lihasaineet.
142. Sydänlihaksen kemiallisen koostumuksen ja aineenvaihdunnan ominaisuudet.
143. Sidekudos. Kollageenin ja elastiinin rakenne ja rakenne, ominaisuudet, biologinen rooli. C-vitamiinin rooli kollageenin biosynteesissä.
144. Sidekudos. Solujen välinen matriisi. Glykosaminoglykaanit, proteoglykaanit ja glykoproteiinit. Rakenne, toiminnot, edustajat. Laadullinen testi sulfatoiduille glykosaminoglykaaneille virtsassa. Määritelmän diagnostinen arvo.
145. Luukudos: mineraalinen ja orgaaninen koostumus. Luukudoksen toiminnot.
146. Biokemialliset muutokset sidekudoksessa ikääntymisen ja joidenkin patologisten prosessien aikana.
147. Maksan biokemia. Aineenvaihdunnan ominaisuudet, rooli kehon elämässä.
148. munuaisten eritystoiminto. diureesin ominaisuudet. Virtsan fysikaalis-kemialliset parametrit.
149. Virtsan yleiset ominaisuudet: diureesi, väri, läpinäkyvyys, reaktio, tiheys. Normin vaihtelut ja patologia. Opiskelumenetelmät.
150. Virtsan kemiallinen koostumus: orgaaniset ja epäorgaaniset komponentit.
151. Virtsan patologiset komponentit: proteiini, veri, ketoaineet, bilirubiini. Esiintymisen syyt, havaitsemismenetelmät.
152. Typen aineenvaihdunnan lopputuotteiden ominaisuudet. Kreatiniinin kvantitatiivinen määritys verestä.
Samanlaisia tietoja.
Moduulin rakenne | Aiheet |
Modulaarinen yksikkö 1 | 11.1. Hormonien rooli aineenvaihdunnan säätelyssä 11.2. Mekanismit hormonaalisten signaalien välittämiseksi soluihin 11.3. Hormonien rakenne ja synteesi 11.4. Pääenergian kantajien vaihdon säätely normaalilla ravitsemusrytmillä 11.5. Muutokset aineenvaihdunnassa hormonien hypo- ja liikaerityksen aikana |
Modulaarinen yksikkö 2 | 11.6. Muutokset hormonaalisessa tilassa ja aineenvaihdunnassa paaston aikana 11.7. Muutokset hormonaalisessa tilassa ja aineenvaihdunnassa diabetes mellituksessa |
Modulaarinen yksikkö 3 | 11.8. Vesi-suola-aineenvaihdunnan säätely 11.9. Kalsium- ja fosfaattiaineenvaihdunnan säätely. Lisäkilpirauhashormonin, kalsitriolin ja kalsitoniinin rakenne, synteesi ja vaikutusmekanismi |
Modulaarinen yksikkö 1 HORMONIEN ROOLI AIBAN SÄÄTELYYN. HIILILIPIDEJEN, LIPIDEJEN, AMINOHAPPOJEN AIHEUDEN SÄÄTELY NORMAALIN RUOVINTARYTMIIN
Oppimistavoitteet Kykyä:
1. Käytä tietoa aineenvaihdunnan ja kehon toimintojen säätelyn molekyylimekanismeista ymmärtääksesi homeostaasin ja sopeutumisen biokemialliset perusteet.
2. Käyttää tietoa hormonien toimintamekanismeista (insuliini ja kontrainsulaarihormonit: glukagoni, kortisoli, adrenaliini, somatotropiini, jodityroniinit) karakterisoidakseen energia-aineenvaihdunnan muutoksia ruoansulatusjaksojen ja imeytymisen jälkeisen tilan muuttuessa.
3. Analysoi aineenvaihdunnan muutokset kortisolin ja kasvuhormonin hypo- ja hypertuotannon aikana, Itsenko-Cushingin tauti ja oireyhtymä (akromegalia) sekä kilpirauhasen hyper- ja hypofunktio (diffuusi toksinen struuma, endeeminen struuma).
Tietää:
1. Nykyaikainen hormonien nimikkeistö ja luokittelu.
2. Hormonaalisten signaalien soluun siirtymisen päävaiheet.
3. Insuliinin ja tärkeimpien kontrasuolahormonien synteesin ja erityksen vaiheet.
4. Mekanismit tärkeimpien energiankantajien pitoisuuden ylläpitämiseksi veressä
vasikoita, joilla on normaali ravintorytmi.
Aihe 11.1. HOMONIEN ROOLI aineenvaihdunnan säätelyssä
1. Monisoluisen organismin normaalille toiminnalle tarvitaan yksittäisten solujen, kudosten ja elinten välinen suhde. Tämä suhde toteutetaan:
hermosto(keskus- ja perifeerinen) hermoimpulssien ja välittäjäaineiden kautta;
endokriiniset järjestelmät endokriinisten rauhasten ja hormonien kautta, jotka näiden rauhasten erikoistuneet solut syntetisoivat, vapautuvat vereen ja kuljetetaan eri elimiin ja kudoksiin;
parakriininen ja autokriininen järjestelmät erilaisten yhdisteiden kautta, jotka erittyvät solujen väliseen tilaan ja ovat vuorovaikutuksessa joko lähellä olevien solujen tai saman solun reseptoreiden kanssa (prostaglandiinit, maha-suolikanavan hormonit, histamiini jne.);
immuunijärjestelmää spesifisten proteiinien (sytokiinit, vasta-aineet) kautta.
2. Endokriininen järjestelmä varmistaa aineenvaihdunnan säätelyn ja integroitumisen eri kudoksissa vasteena ulkoisen ja sisäisen ympäristön olosuhteiden muutoksiin. Hormonit toimivat kemiallisina sanansaattajina, jotka kuljettavat tietoa näistä muutoksista eri elimiin ja kudoksiin. Solun vaste hormonin toimintaan määräytyy sekä hormonin kemiallisen rakenteen että solutyypin mukaan, johon sen vaikutus kohdistuu. Hormoneja on veressä hyvin pieninä pitoisuuksina ja niiden vaikutus on yleensä lyhytaikainen.
Tämä johtuu ensinnäkin niiden synteesin ja erittymisen säätelystä ja toiseksi verenkierrossa olevien hormonien korkeasta inaktivaationopeudesta. Tärkeimmät yhteydet hermoston ja endokriinisen säätelyjärjestelmän välillä suoritetaan aivojen erityisten osien - hypotalamuksen ja aivolisäkkeen - avulla. Neurohumoraalisella säätelyjärjestelmällä on oma hierarkia, jonka huippu on keskushermosto ja prosessien tiukka järjestys.
3. Sääntelyjärjestelmien hierarkia. Aineenvaihduntaa ja kehon toimintoja säätelevät järjestelmät muodostavat kolme hierarkkista tasoa (kuva 11.1).
Ensimmäinen taso- keskushermosto. Hermosolut vastaanottavat signaaleja ulkoisesta ja sisäisestä ympäristöstä, muuntaa ne hermoimpulssin muotoon, joka synapsissa aiheuttaa välittäjän vapautumisen. Mediaattorit aiheuttavat metabolisia muutoksia efektorisoluissa solunsisäisten säätelymekanismien kautta.
Toinen taso- endokriiniset järjestelmät- sisältää hypotalamuksen, aivolisäkkeen, perifeeriset endokriiniset rauhaset sekä joidenkin elinten ja kudosten erikoistuneet solut (ruoansulatuskanava, rasvasolut), jotka syntetisoivat hormoneja ja vapauttavat niitä vereen sopivan ärsykkeen vaikutuksesta.
Kolmas taso- solunsisäinen- muodostavat muutoksia aineenvaihdunnassa solussa tai tietyssä aineenvaihduntareitissä, jotka johtuvat:
Muutokset toiminta entsyymit aktivoimalla tai estämällä;
Muutokset määriä entsyymit proteiinisynteesin induktio- tai tukahduttamismekanismilla tai muutoksilla niiden hajoamisnopeudessa;
Muutokset kuljetusnopeus aineet solukalvojen läpi. Synteesi ja hormonien eritystä ulkoinen ja sisäinen stimuloi
signaaleja keskushermostoon. Nämä signaalit hermoyhteyksien kautta tulevat hypotalamukseen, missä ne stimuloivat peptidihormonien (niin sanottujen vapauttavien hormonien) - liberiinien ja statiinien - synteesiä. Liberialaiset ja statiinit Kuljetetaan aivolisäkkeen etuosaan, missä ne stimuloivat tai estävät trooppisten hormonien synteesiä. Aivolisäkkeen trooppiset hormonit stimuloivat hormonien synteesiä ja erittymistä perifeerisistä endokriinisistä rauhasista, jotka tulevat yleiseen verenkiertoon. Jotkut hypotalamuksen hormonit varastoituvat aivolisäkkeen takaosaan, josta ne erittyvät vereen (vasopressiini, oksitosiini).
 Negatiivisen palautemekanismin aiheuttama muutos aineenvaihduntatuotteiden pitoisuudessa kohdesoluissa estää hormonien synteesiä, jotka vaikuttavat joko umpieritysrauhasiin tai hypotalamukseen; perifeeristen rauhasten hormonit estävät trooppisten hormonien synteesiä ja erittymistä.
Negatiivisen palautemekanismin aiheuttama muutos aineenvaihduntatuotteiden pitoisuudessa kohdesoluissa estää hormonien synteesiä, jotka vaikuttavat joko umpieritysrauhasiin tai hypotalamukseen; perifeeristen rauhasten hormonit estävät trooppisten hormonien synteesiä ja erittymistä.
AIHE 11.2. HORMONAALISTEN SIGNAALIEN SIIRTYMISMEKANISMIT SOLUIHIN
Hormonien biologinen toiminta ilmenee niiden vuorovaikutuksessa solujen kanssa, joilla on tämän hormonin reseptoreita (kohdesolut). Jotta biologinen aktiivisuus olisi aktiivista, hormonin sitoutumisen reseptoriin täytyy johtaa kemialliseen signaaliin solussa, joka saa aikaan spesifisen biologisen vasteen, kuten muutoksen entsyymien ja muiden proteiinien synteesin nopeudessa tai muutoksessa niiden (katso moduuli 4). Hormonin kohde voi toimia yhden tai useamman kudoksen soluina. Kohdesoluun vaikuttaessaan hormoni aiheuttaa spesifisen vasteen, jonka ilmeneminen riippuu siitä, mitkä aineenvaihduntareitit tässä solussa aktivoituvat tai estyvät. Esimerkiksi kilpirauhanen on erityinen kohde tyrotropiinille, joka lisää kilpirauhasen akinaarisolujen määrää ja lisää kilpirauhashormonien biosynteesiä. Glukagoni, joka vaikuttaa rasvasoluihin, aktivoi lipolyysiä, stimuloi glykogeenin mobilisaatiota ja glukoneogeneesiä maksassa.
Reseptorit hormonit voivat sijaita joko plasmakalvossa tai solun sisällä (sytosolissa tai tumassa).
Vaikutusmekanismin mukaan Hormonit voidaan jakaa kahteen ryhmään:
Vastaanottaja ensimmäinen Tähän ryhmään kuuluvat hormonit, jotka ovat vuorovaikutuksessa kalvoreseptorit(peptidihormonit, adrenaliini sekä paikallisen vaikutuksen hormonit - sytokiinit, eikosanoidit);
- toinen ryhmään kuuluvat hormonit, jotka ovat vuorovaikutuksessa solunsisäiset reseptorit- steroidihormonit, tyroksiini (katso moduuli 4).
Hormonin (ensisijainen lähetti) sitoutuminen reseptoriin johtaa muutokseen reseptorin konformaatiossa. Nämä muutokset vangitsevat muut makromolekyylit, ts. hormonin sitoutuminen reseptoriin johtaa joidenkin molekyylien pariutumiseen toisten kanssa (signaalin transduktio). Siten syntyy signaali, joka säätelee soluvastetta. Riippuen hormonaalisen signaalin lähetystavasta solujen metabolisten reaktioiden nopeus muuttuu:
Entsyymien aktiivisuuden muutosten seurauksena;
Entsyymien lukumäärän muutoksen seurauksena (kuva 11.2).
 Riisi. 11.2. Tärkeimmät vaiheet hormonaalisten signaalien välittämisessä kohdesoluihin
Riisi. 11.2. Tärkeimmät vaiheet hormonaalisten signaalien välittämisessä kohdesoluihin
AIHE 11.3. HORMONIEN RAKENNE JA BIOSYNTEESI
1. Peptidihormonit syntetisoituu, kuten muutkin proteiinit, translaatioprosessissa aminohapoista. Jotkut peptidihormonit ovat lyhyitä peptidejä; esimerkiksi hypotalamuksen hormoni tyrotropiini-liberiini-tripeptidi. Useimmat aivolisäkkeen etuosan hormonit ovat glykoproteiineja.
Jotkut peptidihormonit ovat yhteisen geenin tuotteita (kuva 11.3). Useimmat polypeptidihormonit syntetisoidaan inaktiivisina prekursoreina - preprohormoneina. Aktiivisten hormonien muodostuminen tapahtuu osittaisella proteolyysillä.
2. Insuliini- polypeptidi, joka koostuu kahdesta polypeptidiketjusta. Ketju A sisältää 21 aminohappotähdettä, ketju B - 30 aminohappotähdettä. Molemmat ketjut on yhdistetty kahdella disulfidisillalla. Insuliinimolekyyli sisältää myös molekyylinsisäisen disulfidisillan A-ketjussa.
insuliinin biosynteesi Se alkaa inaktiivisten esiasteiden, preproinsuliinin ja proinsuliinin, muodostumisella, jotka muuttuvat peräkkäisen proteolyysin seurauksena aktiiviseksi hormoniksi. Preproinsuliinin biosynteesi alkaa signaalipeptidin muodostumisesta polyribosomeille, jotka liittyvät endoplasmiseen retikulumiin. Signaali
 Riisi. 11.3. Peptidihormonien muodostuminen, jotka ovat yhteisen geenin tuotteita:
Riisi. 11.3. Peptidihormonien muodostuminen, jotka ovat yhteisen geenin tuotteita:
A - POMC (proopiomelanokortiini) syntetisoituu aivolisäkkeen etu- ja välilohkoissa sekä joissakin muissa kudoksissa (suoli, istukka). Polypeptidiketju koostuu 265 aminohappotähteestä; B - N-terminaalisen signaalipeptidin katkaisun jälkeen polypeptidiketju jaetaan kahdeksi fragmentiksi: ACTH (39 a.k.) ja p-lipotropiini (42-134 a.k.); C, D, E - lisäproteolyysin myötä tapahtuu α- ja β-MSH:n (melanosyyttiä stimuloivan hormonin) ja endorfiinien muodostumista. CPPDH on aivolisäkkeen välilohkon kortikotropiinin kaltainen hormoni. POMC-käsittely aivolisäkkeen etu- ja välilohkoissa etenee eri tavalla, jolloin muodostuu erilainen peptidisarja.
peptidi tunkeutuu endoplasmisen retikulumin onteloon ja ohjaa kasvavan polypeptidiketjun ER:hen. Kun preproinsuliinin synteesi on saatu päätökseen, signaalipeptidi katkaistaan (kuva 11.4).
Proinsuliini (86 aminohappotähdettä) tulee Golgin laitteistoon, jossa se pilkkoutuu spesifisten proteaasien vaikutuksesta useisiin kohtiin, jolloin muodostuu insuliinia (51 aminohappotähdettä) ja C-peptidiä, joka koostuu 31 aminohappotähteestä. Insuliini ja C-peptidi sisällytetään erittäviin rakeisiin ekvimolaarisina määrinä. Rakeissa insuliini yhdistyy sinkin kanssa muodostaen dimeerejä ja heksameereja. Kypsät rakeet fuusioituvat plasmakalvon kanssa ja insuliini ja C-peptidi erittyvät solunulkoiseen nesteeseen eksosytoosin kautta. Vereen erittymisen jälkeen insuliinioligomeerit hajoavat. Insuliinin puoliintumisaika plasmassa on 3-10 minuuttia, C-peptidin - noin 30 minuuttia. Insuliinin hajoaminen tapahtuu insulinaasientsyymin vaikutuksesta pääasiassa maksassa ja vähäisemmässä määrin munuaisissa.
Pääasiallinen insuliinisynteesin ja -erityksen stimulaattori on glukoosi. Insuliinin eritystä lisäävät myös tietyt aminohapot (erityisesti arginiini ja lysiini), ketoaineet ja rasvahapot. Adrenaliini, somatostatiini ja jotkut maha-suolikanavan peptidit estävät insuliinin eritystä.
 Riisi. 11.4. Insuliinin biosynteesin kaavio haiman soluissa:
Riisi. 11.4. Insuliinin biosynteesin kaavio haiman soluissa:
1 - proinsuliinin polypeptidiketjun synteesi; 2 - synteesi tapahtuu polyribosomeissa, jotka ovat kiinnittyneet ER-kalvon ulkopintaan; 3 - signaalipeptidi katkaistaan pois polypeptidiketjun synteesin päätyttyä ja proinsuliini muodostuu; 4 - proinsuliini kuljetetaan ER:stä Golgin laitteeseen ja pilkkoutuu insuliiniksi ja C-peptidiksi; 5 - insuliini ja C-peptidi liitetään erittyviin rakeisiin ja vapautuvat eksosytoosin kautta (6); ER - endoplasminen verkkokalvo; N on molekyylin pääteosa;
3. Glukagoni- yksiketjuinen polypeptidi, joka koostuu 29 aminohappotähteestä. Glukagonin biosynteesi tapahtuu Langerhansin saarekkeiden α-soluissa preproglukagonin inaktiivisesta prekursorista, joka osittaisen proteolyysin seurauksena muuttuu aktiiviseksi hormoniksi. Glukoosi ja insuliini estävät glukagonin eritystä; monet yhdisteet, mukaan lukien aminohapot, rasvahapot, välittäjäaineet (adrenaliini), stimuloivat sitä. Hormonin puoliintumisaika on ~5 minuuttia. Maksassa glukagoni hajoaa nopeasti spesifisten proteaasien vaikutuksesta.
4. Somatotropiini syntetisoituu prohormonina somatotrofisissa soluissa, joita on eniten aivolisäkkeen etuosassa. Kaikkien nisäkäslajien kasvuhormoni on yksiketjuinen
molekyylipainoltaan 22 kDa:n peptidi, joka koostuu 191 aminohappotähteestä ja jossa on kaksi molekyylinsisäistä disulfidisidosta. Kasvuhormonin eritys sykkii 20-30 minuutin välein. Yksi suurimmista huipuista havaitaan pian nukahtamisen jälkeen. Erilaisten ärsykkeiden (liikunta, paasto, proteiiniruoat, aminohappo arginiini) vaikutuksesta jopa ei-kasvavilla aikuisilla veren kasvuhormonin taso voi nousta arvoon 30-100 ng / ml. Kasvuhormonin synteesiä ja eritystä säätelevät monet tekijät. Pääasiallinen stimuloiva vaikutus on somatoliberiinilla, pääasiallinen estävä vaikutus on hypotalamuksen somatostatiini.
5. Jodityroniinit syntetisoituu osana proteiinia - tyroglobuliini (Tg)
 Riisi. 11.5. Jodityroniinien synteesi:
Riisi. 11.5. Jodityroniinien synteesi:
ER - endoplasminen verkkokalvo; DIT - dijodityroniini; Tg - tyroglobuliini; T3 - trijodityroniini, T4 - tyroksiini. Tyroglobuliini syntetisoituu ribosomeissa, menee sitten Golgi-kompleksiin ja sitten solunulkoiseen kolloidiin, jossa se varastoituu ja jossa tyrosiinijäännökset jodataan. Jodityroniinien muodostuminen tapahtuu useissa vaiheissa: jodin kuljetus kilpirauhasen soluihin, jodin hapettuminen, tyrosiinijäämien jodautuminen, jodityroniinien muodostuminen, jodityroniinien kuljetus vereen
tyroglobuliini- glykoproteiini, sisältää 115 tyrosiinitähdettä, syntetisoituu solun tyviosassa ja varastoituu solunulkoiseen kolloidiin, jossa tyrosiinitähteet jodataan ja jodityroniinit muodostuvat.
Vaikutuksen alaisena tyroperoksidaasi hapetettu jodi reagoi tyrosiinijäänteiden kanssa muodostaen monojodityroniineja (MIT) ja dijodityroniineja (DIT). Kaksi DIT-molekyyliä kondensoituu muodostaen T4:n ja MIT ja DIT tiivistyvät muodostaen T3:a. Jodtyroglobuliini kuljetetaan soluun endosytoosin kautta ja hydrolysoituu lysosomientsyymien toimesta vapauttaen T3:a ja T4:ää (kuva 11.6).
 Riisi. 11.6. Kilpirauhashormonien rakenne
Riisi. 11.6. Kilpirauhashormonien rakenne
T3 on jodityroniinien tärkein biologisesti aktiivinen muoto; sen affiniteetti kohdesolureseptoriin on 10 kertaa suurempi kuin T4:n. Ääreiskudoksissa T4-osan dejodaation seurauksena viidennessä hiiliatomissa muodostuu T3:n niin kutsuttu "käänteinen" muoto, joka on lähes täysin vailla biologista aktiivisuutta.
Jodityroniinit ovat veressä sitoutuneessa muodossa kompleksina tyroksiinia sitovan proteiinin kanssa. Vain 0,03 % T4:stä ja 0,3 % T3:sta on vapaassa tilassa. Jodityroniinien biologinen aktiivisuus johtuu sitoutumattomasta fraktiosta. Kuljetusproteiinit toimivat eräänlaisena varastona, josta voi saada lisämäärää vapaita hormoneja. Jodityroniinien synteesiä ja eritystä säätelee hypotalamus-aivolisäkejärjestelmä
 Riisi. 11.7. Jodityroniinien synteesin ja erityksen säätely:
Riisi. 11.7. Jodityroniinien synteesin ja erityksen säätely:
1 - tyrotropiini-liberiini stimuloi TSH:n vapautumista; 2 - TSH stimuloi jodityroniinien synteesiä ja eritystä; 3, 4 - jodotyroniinit estävät TSH:n synteesiä ja erittymistä
Jodityroniinit säätelevät kahden tyyppisiä prosesseja:
Kudosten kasvu ja erilaistuminen;
Energian vaihto.
6. Kortikosteroidit. Kaikkien kortikosteroidien yleinen esiaste on kolesteroli. Kolesterolin lähde kortikosteroidien synteesiä varten on sen esterit, jotka tulevat soluun osana LDL:ää tai kerrostuvat soluun. Kortikotropiini stimuloi kolesterolin vapautumista estereistään ja kortikosteroidien synteesiä. Kortisolin synteesireaktioita esiintyy lisämunuaiskuoren solujen eri osastoissa (ks. kuva 11.12). Kortikosteroidien synteesin aikana muodostuu yli 40 metaboliittia, jotka eroavat rakenteeltaan ja biologiselta aktiivisuudeltaan. Tärkeimmät kortikosteroidit, joilla on voimakas hormonaalinen aktiivisuus, ovat kortisoli, glukokortikoidiryhmän pääedustaja, aldosteroni, tärkein mineralokortikoidi, ja androgeenit.
Kortikosteroidien synteesin ensimmäisessä vaiheessa kolesteroli muuttuu pregnenoloniksi irrottamalla 6-hiilifragmentti kolesterolin sivuketjusta ja hapettamalla hiiliatomi C 20 . Pregnenoloni muuttuu progesteroniksi - steroidien C 21 -prekursoriksi - kortisoliksi ja aldosteroniksi - ja C 19 -steroideiksi - androgeenien esiasteiksi. Se, millainen steroidi on lopputuote, riippuu solun entsyymijoukosta ja hydroksylaatioreaktioiden sekvenssistä (kuva 11.8).
 Riisi. 11.8. Tärkeimpien kortikosteroidien synteesi:
Riisi. 11.8. Tärkeimpien kortikosteroidien synteesi:
1 - kolesterolin muuntaminen pregnenoloniksi; 2 - progesteronin muodostuminen;
progesteronin 3-hydroksylaatio (17-21-11) ja kortisolin muodostuminen;
4 - progesteronin (21-11) hydroksylaatio ja aldosteronin muodostuminen;
5 - androgeenisynteesireitti
Progesteronin primaarinen hydroksylaatio 17-hydroksylaasilla ja sitten 21- ja 11-hydroksylaasilla johtaa kortisolin synteesiin. Aldosteronin muodostumisreaktioihin liittyy progesteronin hydroksylaatio ensin 21-hydroksylaasilla ja sitten 11-hydroksylaasilla (katso kuva 11.8). Kortisolin synteesin ja erittymisen nopeutta säätelee hypotalamus-aivolisäkejärjestelmä negatiivisen palautemekanismin avulla (kuva 11.9).
Steroidihormonit kuljetetaan veren mukana yhdessä tiettyjen kuljetusproteiinien kanssa.
Katabolismi lisämunuaiskuoren hormoneja esiintyy pääasiassa maksassa. Hydroksylaation, hapettumisen ja
 Riisi. 11.9. Kortisolin synteesin ja erittymisen säätely:
Riisi. 11.9. Kortisolin synteesin ja erittymisen säätely:
1 - kortikotropiini-liberiinin synteesin stimulointi; 2 - kortikotropinliberiini stimuloi ACTH:n synteesiä ja eritystä; 3 - ACTH stimuloi kortisolin synteesiä ja eritystä; 4 - kortisoli estää ACTH:n ja kortikoliberiinin erittymistä
hormonien palautuminen. Kortikosteroidien kataboliatuotteet (paitsi kortikosteroni ja aldosteroni) erittyvät virtsaan 17-ketosteroidit. Nämä aineenvaihduntatuotteet erittyvät pääasiassa konjugaattien muodossa glukuroni- ja rikkihapon kanssa. Miehillä 2/3 ketosteroideista muodostuu kortikosteroideista ja 1/3 testosteronista (vain 12-17 mg päivässä). Naisilla 17-ketosteroideja muodostuu pääasiassa kortikosteroidien vaikutuksesta (7-12 mg päivässä).
AIHE 11.4. PERUSENERGIAN KANTOJEN VAIHDON SÄÄTÖ NORMAALIRYTMIIN
RUOKA
1. Pääravinteiden energia-arvo ilmaistaan kilokaloreina ja on: hiilihydraateille - 4 kcal / g, rasvoille - 9 kcal / g, proteiineille - 4 kcal / g. Aikuinen terve ihminen tarvitsee 2000-3000 kcal (8000-12000 kJ) energiaa vuorokaudessa.
Tavanomaisella ravitsemusrytmillä aterioiden välit ovat 4-5 tuntia 8-12 tunnin yötauolla. ruoansulatuksen aikana ja imeytymisaika(2-4 tuntia) pääasialliset kudosten käyttämät energian kantajat (glukoosi, rasvahapot, aminohapot) pääsevät vereen suoraan ruoansulatuskanavasta. AT postabsorptiivinen ajanjakso(aikajakso ruoansulatuksen päättymisen jälkeen seuraavaan ateriaan) ja nälkään näkemisen aikana muodostuu energiasubstraatteja
kerrostuneiden energiankantajien hajoamisprosessissa. Päärooli näiden prosessien säätelyssä on insuliinia ja glukagoni. Myös insuliiniantagonistit ovat adrenaliini, kortisoli, jodityroniinit ja somatotropiini
(ns. kontrainsulaariset hormonit).
Insuliini ja kontrainsulaariset hormonit tarjoavat tasapainon kehon tarpeiden ja kykyjen välillä saada normaaliin toimintaan ja kasvuun tarvittavaa energiaa. Tämä saldo määritellään seuraavasti energian homeostaasi. Normaalilla ruokailurytmillä veren glukoosipitoisuus pysyy tasolla 65-110 mg / dl (3,58-6,05 mmol / l) kahden päähormonin - insuliinin ja glukagonin - vaikutuksesta. Insuliini ja glukagoni ovat tärkeimmät aineenvaihdunnan säätelijät ruoansulatuksen vaihtuvien tilojen, imeytymisen jälkeisen ajanjakson ja nälänhädän aikana. Ruoansulatusjaksot ovat 10-15 tuntia vuorokaudessa ja energiankulutus tapahtuu 24 tunnin sisällä. Siksi osa ruoansulatuksen aikana olevista energian kantajista varastoidaan käytettäväksi imeytymisen jälkeisenä aikana.
Maksa, rasvakudos ja lihakset ovat tärkeimpiä elimiä, jotka tuottavat aineenvaihdunnan muutoksia ravitsemusrytmin mukaisesti. Varastointitila aktivoituu aterian jälkeen ja korvataan varannon mobilisointitilalla imeytymisjakson päätyttyä.
2. Muutokset tärkeimpien energiankantajien aineenvaihdunnassa absorptiojakson aikana pääasiassa korkean vuoksi insuliini-glukagoni indeksi
(Kuva 11.10).
Maksassa glukoosin kulutus kasvaa, mikä on seurausta aineenvaihduntareittien kiihtymisestä, jossa glukoosi muuttuu energian kantajiksi kerrostuneiksi muodoiksi: glykogeeni ja rasvat.
Kun glukoosin pitoisuus hepatosyyteissä kasvaa, glukokinaasi aktivoituu, mikä muuntaa glukoosin glukoosi-6-fosfaatiksi. Lisäksi insuliini indusoi glukokinaasi-mRNA:n synteesiä. Tämän seurauksena glukoosi-6-fosfaatin pitoisuus maksasoluissa kasvaa, mikä aiheuttaa kiihtyvyyttä glykogeenisynteesi. Tätä helpottaa myös glykogeenifosforylaasin samanaikainen inaktivoituminen ja glykogeenisyntaasin aktivaatio. Insuliini vaikuttaa maksasoluissa nopeuttaa glykolyysiä keskeisten entsyymien, glukokinaasin, fosfofruktokinaasin ja pyruvaattikinaasin, aktiivisuuden ja lukumäärän lisääntymisen seurauksena. Samaan aikaan glukoneogeneesi estyy fruktoosi-1,6-bisfosfataasin inaktivoinnin ja glukoneogeneesin avainentsyymien, fosfsynteesin insuliinirepression seurauksena (katso moduuli 6).
Glukoosi-6-fosfaatin pitoisuuden nousu maksasoluissa imeytymisjakson aikana yhdistetään NADPH:n aktiiviseen käyttöön rasvahappojen synteesiin, mikä edistää stimulaatiota pentoosifosfaattireitti.
Rasvahapposynteesin kiihtyminen Sen varmistavat glukoosiaineenvaihdunnan aikana muodostuvien substraattien (asetyyli-CoA ja NADPH) saatavuus sekä insuliinin rasvahapposynteesin avainentsyymien aktivointi ja induktio.
 Riisi. 11.10. Tapoja käyttää tärkeimpiä energiankantajia absorptiojakson aikana:
Riisi. 11.10. Tapoja käyttää tärkeimpiä energiankantajia absorptiojakson aikana:
1 - glykogeenin biosynteesi maksassa; 2 - glykolyysi; 3 - TAG-biosynteesi maksassa; 4 - TAG-biosynteesi rasvakudoksessa; 5 - glykogeenin biosynteesi lihaksissa; 6 - proteiinien biosynteesi eri kudoksissa, mukaan lukien maksa; FA - rasvahapot
Ruoansulatuskanavasta maksaan tulevia aminohappoja käytetään syntetisoimaan proteiineja ja muita typpeä sisältäviä yhdisteitä, ja niiden ylimäärä joko päätyy verenkiertoon ja kuljetetaan muihin kudoksiin tai deaminoituu, minkä jälkeen typpivapaat jäämät sisällytetään yleinen katabolian reitti (katso moduuli 9).
Adiposyyttien metaboliset muutokset. Rasvakudoksen päätehtävä on varastoida energian kantajia muodossa triasyyliglyserolit. glukoosin kuljetus adiposyytteihin. Solunsisäisen glukoosipitoisuuden kasvu ja glykolyysin avainentsyymien aktivoituminen saavat aikaan asetyyli-CoA:n ja glyseroli-3-fosfaatin muodostumisen, jotka ovat välttämättömiä TAG:n synteesille. Pentoosifosfaattireitin stimulaatio saa aikaan NADPH:n muodostumisen, joka on välttämätön rasvahappojen synteesille. Kuitenkin de novo rasvahappojen biosynteesi ihmisen rasvakudoksessa etenee suurella nopeudella vasta edeltävän paaston jälkeen. Normaalin ruokintarytmin aikana TAG-synteesi perustuu pääasiassa kylomikroneista ja VLDL:stä Lp-lipaasin vaikutuksesta tuleviin rasvahappoihin (katso moduuli 8).
Koska hormoniherkkä TAG-lipaasi absorptiotilassa on defosforyloituneessa, inaktiivisessa muodossa, lipolyysiprosessi estyy.
Muutokset lihasten aineenvaihdunnassa. Insuliinin vaikutuksen alaisena kiihtyy glukoosin kuljetus lihassoluihin. Glukoosi fosforyloidaan ja hapetetaan energian tuottamiseksi soluille, ja sitä käytetään myös glykogeenin syntetisoimiseen. Tänä aikana kylomikroneista ja VLDL:stä tulevilla rasvahapoilla on merkityksetön rooli lihasten energia-aineenvaihdunnassa. Aminohappojen virtaus lihaksiin ja proteiinien biosynteesi lisääntyy myös insuliinin vaikutuksesta, erityisesti proteiiniruokien nauttimisen jälkeen ja lihastyön aikana.
3. Muutokset pääenergian kantajien aineenvaihdunnassa, kun absorptiotila muuttuu postabsorptiiviseksi. Postabsorptiojaksolla, kun insuliini-glukagoni-indeksi laskee, aineenvaihdunnan muutokset tähtäävät pääasiassa veren glukoosipitoisuuden ylläpitämiseen, joka toimii aivojen pääasiallisena energiasubstraattina ja erytrosyyttien ainoana energialähteenä. Tärkeimmät muutokset aineenvaihdunnassa tänä aikana tapahtuvat maksassa ja rasvakudoksessa (kuva 11.11), ja niiden tarkoituksena on täydentää glukoosia sisäisistä varannoista ja käyttää muita energiasubstraatteja (rasvoja ja aminohappoja).
Metaboliset muutokset maksassa. Glukagonin vaikutuksen alaisena kiihtyy glykogeenin mobilisaatio(katso moduuli 6). Maksan glykogeenivarastot tyhjenevät 18-24 tunnin paaston aikana. Pääasiallinen glukoosin lähde glykogeenivarastojen loppuessa tulee glukoneogeneesi, joka alkaa kiihtyä 4-6 tuntia viimeisen aterian jälkeen. Glukoosisynteesin substraatit ovat laktaatti, glyseroli ja aminohappoja. Rasvahapposynteesin nopeus laskee johtuen asetyyli-CoA-karboksylaasin fosforylaatiosta ja inaktivoitumisesta fosforylaation aikana, ja β-hapetuksen nopeus kasvaa. Samalla lisääntyy maksan rasvahappojen saanti, jotka kulkeutuvat rasvavarastoista kiihtyneen lipolyysin seurauksena. Rasvahappojen hapettumisen aikana muodostuvaa asetyyli-CoA:ta käytetään maksassa ketoaineiden synteesi.
rasvakudoksessa TAG-synteesin nopeus laskee ja lipolyysi stimuloituu. Lipolyysin stimulaatio on seurausta hormoniherkän adiposyytti-TAG-lipaasin aktivaatiosta glukagonin vaikutuksen alaisena. Rasvahapoista tulee tärkeitä energianlähteitä maksassa, lihaksissa ja rasvakudoksessa.
Siten imeytymisen jälkeisenä aikana veren glukoosin pitoisuus pysyy tasolla 60-100 mg / dl (3,5-5,5 mmol / l), ja rasvahappojen ja ketoaineiden taso nousee.
 Riisi. 11.11. Tapoja käyttää pääenergian kantajia vaihdettaessa absorptiotilasta jälkiabsorptiotilaan:
Riisi. 11.11. Tapoja käyttää pääenergian kantajia vaihdettaessa absorptiotilasta jälkiabsorptiotilaan:
I - insuliini-glukagoniindeksin lasku; 2 - glykogeenin hajoaminen; 3, 4 - glukoosin kuljetus aivoihin ja punasoluihin; 5 - rasvojen katabolia; 6 - rasvojen kuljetus maksaan ja lihaksiin; 7 - ketoaineiden synteesi maksassa; 8 - ketoaineiden kuljetus lihaksiin; 9 - glukoneogeneesi aminohapoista; 10 - urean synteesi ja erittyminen;
II - laktaatin kuljetus maksaan ja sisällyttäminen glukoneogeneesiin; 12 - glukoneogeneesi glyserolista; KT - ketonikappaleet; FA - rasvahapot
AIHE 11.5. MUUTOKSET AINEENVAIHTOESSA HORMONIEN HYPO- JA HYPERERITTUMISEN AIKANA
Muutos hormonien synteesin ja erittymisen nopeudessa voi tapahtua paitsi mukautuvana prosessina, joka tapahtuu vastauksena kehon fysiologisen toiminnan muutokseen, vaan usein seurauksena umpieritysrauhasten toiminnallisen toiminnan rikkomuksista patologisten prosessien kehittyminen tai säätelyhäiriöt niissä. Nämä häiriöt voivat ilmetä joko muodossa vajaatoiminta, mikä johtaa hormonin määrän laskuun tai hyperfunktio, liiallinen synteesi.
1. Kilpirauhasen ylitoiminta(kilpirauhasen liikatoiminta) ilmenee useissa kliinisissä muodoissa. Diffuusi myrkyllinen struuma(Gravesin tauti, Gravesin tauti) on yleisin kilpirauhasen sairaus. Tässä taudissa kilpirauhasen (struuma) koko kasvaa, jodityroniinien pitoisuus kasvaa 2-5 kertaa ja tyreotoksikoosi kehittyy.
Tyreotoksikoosin tyypillisiä merkkejä ovat perusaineenvaihdunnan lisääntyminen, sydämen sykkeen lisääntyminen, lihasheikkous, laihtuminen (huolimatta lisääntyneestä ruokahalusta), hikoilu, kuume, vapina ja eksoftalmos (pullisevat silmät). Nämä oireet heijastavat sekä anabolisten (kudosten kasvu ja erilaistuminen) että katabolisten prosessien (hiilihydraattien, lipidien ja selän katabolia) samanaikaista stimulaatiota jodotyroniinien toimesta. Suuremmassa määrin kataboliaprosessit tehostuvat, mistä on osoituksena negatiivinen typpitase. kilpirauhasen liikatoiminta voi johtua useista syistä: kasvaimen kehittyminen, tulehdus (tyreoidiitti), liiallinen jodin ja jodia sisältävien lääkkeiden saanti, autoimmuunireaktiot.
autoimmuuni hypertyreoosi tapahtuu vasta-aineiden muodostumisen seurauksena kilpirauhasta stimuloivan hormonin reseptoreille kilpirauhasessa. Yksi niistä, immunoglobuliini (IgG), jäljittelee tyrotropiinin toimintaa olemalla vuorovaikutuksessa kilpirauhassolujen kalvolla olevien TSH-reseptorien kanssa. Tämä johtaa kilpirauhasen hajanaiseen liikakasvuun ja liialliseen hallitsemattomaan T3:n ja T4:n tuotantoon, koska takaisinkytkentämekanismi ei säätele IgG:n muodostumista. TSH:n taso tässä taudissa on alentunut, koska korkeat jodityroniinipitoisuudet estävät aivolisäkkeen toimintaa.
2. Kilpirauhasen vajaatoiminta voi johtua riittämättömästä jodin saannista kehossa - endeeminen struuma. Harvemmin kilpirauhasen vajaatoimintaa esiintyy jodityroniinien synteesiin osallistuvien entsyymien (esimerkiksi tyroperoksiraasin) synnynnäisten vikojen seurauksena tai muiden sairauksien komplikaationa, jossa hypotalamus, aivolisäke tai kilpirauhanen on vaurioitunut. Joissakin kilpirauhasen vajaatoiminnan muodoissa verestä löytyy vasta-aineita tyroglobuliinille. Varhaislapsuudessa kilpirauhasen vajaatoiminta johtaa fyysisen ja henkisen kehityksen viivästymiseen - kretinismi. Aikuisilla hypofunction ilmenee mm myksedeema(limaturvotus). Myksedeeman pääasiallinen ilmentymä on proteoglykaanien ja veden liiallinen kertyminen ihoon. Kilpirauhasen vajaatoiminnan tärkeimmät oireet: uneliaisuus, kylmänsietokyvyn heikkeneminen, painonnousu, kehon lämpötilan lasku.
3. Hyperkortisolismi. liiallinen kortikosteroidien, pääasiassa kortisolin, muodostuminen, - hyperkortisolismia- usein seurausta kortisolin synteesin säätelymekanismien rikkomisesta:
Aivolisäkkeen kasvain ja lisääntynyt kortikotropiinin tuotanto (Itsenko-Cushingin tauti);
Lisämunuaisen kasvaimet, jotka tuottavat kortisolia (Itsenko-Cushingin oireyhtymä).
Hyperkortismin pääasialliset ilmentymät ovat hyperglukosemia ja alentunut glukoositoleranssi, joka johtuu glukoneogeneesin stimulaatiosta ja kohonneesta verenpaineesta kortisolin mineralokortikoidiaktiivisuuden ja Na+-ionien pitoisuuden nousun seurauksena.
4. Hypokortisismi. Perinnöllinen adrenogenitaalinen dystrofia 95 %:ssa tapauksista se johtuu 21-hydroksylaasin puutteesta (katso kuva 11.8). Tämä lisää 17-OH-progesteronin ja androgeenin tuotantoa. Taudille tyypillisiä oireita ovat varhainen murrosikä pojilla ja miesten sukupuoliominaisuuksien kehittyminen tytöillä. Naisten osittaisen 21-hydroksylaasin puutteen vuoksi kuukautiskierto voi häiriintyä.
Hankittu lisämunuaisen vajaatoiminta voi kehittyä lisämunuaiskuoren solujen tuberkuloosi- tai autoimmuunivaurion ja kortikosteroidien synteesin vähenemisen seurauksena. Lisämunuaisten säätelyn menettäminen johtaa kortikotropiinin lisääntyneeseen erittymiseen. Näissä tapauksissa potilailla on lisääntynyt ihon ja limakalvojen pigmentaatio. (Addisonin tauti) mikä johtuu kortikotropiinin ja muiden POMC-johdannaisten, erityisesti melanosyyttejä stimuloivan hormonin, lisääntyneestä tuotannosta (katso kuva 11.3). Lisämunuaisten vajaatoiminnan tärkeimmät kliiniset ilmenemismuodot: hypotensio, lihasheikkous, hyponatremia, laihtuminen, stressin sietokyky.
Lisämunuaiskuoren toiminnan puute usein seurausta pitkäaikaisesta kortikosteroidilääkkeiden käytöstä, jotka estävät kortikotropiinin synteesiä takaisinkytkentämekanismilla. Stimuloivien signaalien puuttuminen johtaa lisämunuaiskuoren solujen surkastumiseen. Hormonaalisten lääkkeiden äkillisen lopettamisen myötä voi kehittyä akuutti lisämunuaisten vajaatoiminta (ns. "vieroitusoireyhtymä", joka on suuri uhka elämälle, koska siihen liittyy kaikentyyppisten aineenvaihdunnan ja sopeutumisprosessien dekompensaatio). Se ilmenee verisuonten romahtamisesta, vakavasta adynamiasta, tajunnan menetyksestä. Tämä tila johtuu elektrolyyttiaineenvaihdunnan rikkomisesta, mikä johtaa Na +- ja C1 --ionien häviämiseen virtsassa ja kuivumiseen solunulkoisen nesteen häviämisen vuoksi. Muutos ilmenee verensokeritason laskuna, glykogeenivarastojen vähenemisenä maksassa ja luustolihaksissa.
1. Siirrä muistikirjaasi ja täytä taulukko. 11.1.
Taulukko 11.1. Insuliini ja tärkeimmät kontrasulkuhormonit
2. Käyttämällä kuviota 11.4, kirjoita ylös insuliinisynteesin vaiheet. Selitä, mitkä syyt voivat johtaa insuliinin puutteen kehittymiseen? Miksi näissä tapauksissa on mahdollista määrittää C-peptidin pitoisuus verestä diagnoosia varten?
3. Tutki jodityroniinien synteesin kaaviota (kuva 11.5). Kuvaa niiden synteesin päävaiheet ja piirrä kaavio kilpirauhashormonien synteesin ja erityksen säätelystä. Selitä hypo- ja hypertyreoosin tärkeimmät ilmenemismuodot. Miksi veren TSH-tasoa on seurattava jatkuvasti käytettäessä tyroksiinia lääkkeenä?
4. Tutki kortisolin synteesin vaiheiden järjestystä (kuva 11.8). Etsi kaaviosta entsyymien katalysoimat vaiheet, joiden vika on adrenogenitaalisen oireyhtymän syy.
5. Kuvaile kortisolin synteesin solunsisäisen syklin kaaviota alkaen ACTH:n vuorovaikutuksesta reseptorin kanssa (kuva 11.12) ja korvaa numerot niihin osallistuvien proteiinien nimillä.
6. Piirrä kaavio kortikosteroidien synteesin ja erityksen säätelystä. Selitä steroidien vieroitusoireyhtymän syitä ja ilmenemismuotoja.
7. Kuvaile tapahtumasarja, joka johtaa verensokerin nousuun ensimmäisen tunnin aikana aterian jälkeen ja sen palaamiseen lähtötasolle 2 tunnin kuluessa (kuva 11.13). Selitä hormonien rooli näissä tapahtumissa.
8. Analysoi hormonaalisen tilan ja aineenvaihdunnan muutoksia maksassa, rasvakudoksessa ja lihaksissa imeytymisjaksolla (kuva 11.10) ja imeytymisen jälkeisellä jaksolla (kuva 11.11). Nimeä numeroilla merkityt prosessit. Ilmoita säätelyentsyymit ja niiden aktiivisuuden muuttamismekanismi ottaen huomioon, että ensisijainen signaali näiden prosessien stimuloimiseksi on muutos veren glukoosipitoisuudessa ja vastavuoroiset muutokset insuliinin ja glukagonin pitoisuuksissa (kuva 11.11).
 Riisi. 11.12. Kortisolin synteesin solunsisäinen sykli:
Riisi. 11.12. Kortisolin synteesin solunsisäinen sykli:
EHS - kolesteroliesterit; CS - kolesteroli
ITSEHALLINTA TEHTÄVÄT
1. Valitse oikeat vastaukset. Hormonit:
A. Ne ilmentävät vaikutuksensa vuorovaikutuksessa reseptorien kanssa B. Ne syntetisoituvat aivolisäkkeen takalohkossa
B. Muuta entsyymiaktiivisuutta osittaisella proteolyysillä D. Indusoi entsyymisynteesi kohdesoluissa
D. Synteesiä ja eritystä säätelee palautemekanismi
 Riisi. 11.13. Glukoosin (A), insuliinin (B) ja glukagonin (C) pitoisuuksien muutosten dynamiikka hiilihydraattipitoisen aterian jälkeen
Riisi. 11.13. Glukoosin (A), insuliinin (B) ja glukagonin (C) pitoisuuksien muutosten dynamiikka hiilihydraattipitoisen aterian jälkeen
2. Valitse oikea vastaus. Rasvakudoksessa oleva glukagoni aktivoi:
A. Hormoniherkkä TAG-lipaasi B. Glukoosi-6-fosfaattidehydrogenaasi
B. Asetyyli-CoA-karboksylaasi D. LP-lipaasi
D. pyruvaattikinaasi
3. Valitse oikeat vastaukset. Jodityroniinit:
A. Syntetisoitu aivolisäkkeessä
B. Vuorovaikutus solunsisäisten reseptorien kanssa
B. Stimuloi Na:n, Ka-ATPaasin toimintaa
D. Suurina pitoisuuksina ne kiihdyttävät katabolian prosesseja D. Osallistuvat jäähdytysvasteeseen
4. Aseta ottelu:
A. Gravesin tauti B. Myxedema
B. Endeeminen struuma D. Kretinismi
D. Autoimmuuninen kilpirauhastulehdus
1. Esiintyy kilpirauhasen vajaatoiminnan yhteydessä varhaisessa iässä
2. Mukana proteoglykaanien ja veden kertyminen ihoon
3. Se on seurausta immunoglobuliinin muodostumisesta, joka jäljittelee TSH:n toimintaa
5. Valitse oikeat vastaukset.
Imeytymisjaksolle on ominaista:
A. Insuliinipitoisuuden lisääminen veressä B. Rasvojen synteesin nopeuttaminen maksassa
B. Glukoneogeneesin kiihtyminen
D. Glykolyysin kiihtyminen maksassa
D. Glukagonin pitoisuuden lisääminen veressä
6. Valitse oikeat vastaukset.
Maksan insuliinin vaikutuksesta kiihtyy:
A. Proteiinin biosynteesi
B. Glykogeenin biosynteesi
B. Glukoneogeneesi
D. Rasvahappojen biosynteesi D. Glykolyysi
7. Aseta ottelu. Hormoni:
A. Insuliini B. Glukagoni
B. Kortisoli D. Adrenaliini
Tehtävä:
1. Stimuloi rasvojen synteesiä glukoosista maksassa
2. Stimuloi lihasten glykogeenin mobilisaatiota
3. Stimuloi jodityroniinien synteesiä
8. Valitse oikeat vastaukset. Steroidihormonit:
A. Läpäise kohdesoluihin
B. Kuljetetaan veren välityksellä yhdessä tiettyjen proteiinien kanssa
B. Stimuloi proteiinin fosforylaatioreaktioita
D. Ole vuorovaikutuksessa kromatiinin kanssa ja muuta transkription nopeutta D. Osallistu translaatioprosessiin.
9. Valitse oikeat vastaukset. Insuliini:
A. Nopeuttaa glukoosin kuljetusta lihaksiin B. Kiihdyttää glykogeenin synteesiä maksassa
B. Stimuloi lipolyysiä rasvakudoksessa D. Kiihdyttää glukoneogeneesiä
D. Nopeuttaa glukoosin kuljetusta rasvasoluihin
1. A, G, D 6. A, B, D, D
2. MUTTA 7. 1-A, 2-D, 3-D
3. B, C, D, D 8. A, B, D
4. 1-D, 2-B, 3-A 9. A, B, D
5. A, B, D
PERUSKÄSITTEET JA KÄSITTEET
2. Preprohormoni
3. Synteesin ja erityksen ärsykkeet
4. Kohdesolut
5. Reseptorit
6. Sääntelyjärjestelmien hierarkia
7. Autokriininen vaikutusmekanismi
8. Parakriininen vaikutusmekanismi
9. Homeostaasi
10. Imeytymisaika
11. Postabsorptiivinen ajanjakso
12. Sopeutuminen
13. Hypofunktio
14. Hyperfunktio
15. Kontrinsulaariset hormonit
Ratkaista ongelmia
1. Tutkittaessa potilaita, joilla on hyperkortisolin oireita, käytetään toiminnallista testiä deksametasonin "kuormalla" (deksametasoni on kortisolin rakenteellinen analogi). Miten 17-ketosteroidien pitoisuus potilaiden virtsassa muuttuu deksametasonin annon jälkeen, jos hyperkortisolismin syy on:
a) kortikotropiinin liikatuotanto;
b) lisämunuaisten hormonaalisesti aktiivinen kasvain.
2. Viisivuotiaan tytön vanhemmat menivät lääkärikeskukseen konsultaatioon. Tutkimuksen aikana lapsella ilmeni toissijaisia miehen sukupuoliominaisuuksia: lihasten liikakasvua, liiallista karvojen kasvua ja äänen sointitason laskua. ACTH:n taso veressä nousee. Lääkäri diagnosoi adrenogenitaalisen oireyhtymän (lisämunuaiskuoren synnynnäinen toimintahäiriö). Perustele lääkärin diagnoosi. Tätä varten:
a) esittää steroidihormonien synteesikaavio; nimeä tärkeimmät fysiologisesti aktiiviset kortikosteroidit ja ilmoittaa niiden toiminnot;
b) nimeä entsyymit, joiden puutos aiheuttaa edellä kuvatut oireet;
c) osoittavat, minkä kortikosteroidisynteesin tuotteiden muodostuminen lisääntyy tässä patologiassa;
d) Selitä, miksi ACTH:n pitoisuus lapsen veressä on kohonnut.
3. Yksi Addisonin taudin muoto on seuraus lisämunuaiskuoren solujen atrofiasta pitkäaikaisen kortikosteroidihoidon aikana. Taudin tärkeimmät ilmentymät: lihasheikkous, hypoglykemia,
dystrofiset muutokset lihaksissa, alentavat verenpainetta; joissakin tapauksissa tällaisilla potilailla on lisääntynyt ihon ja limakalvojen pigmentaatio. Kuinka selittää taudin luetellut oireet? Selitykseksi:
a) esittää steroidihormonien synteesikaavio; nimeä tärkeimmät fysiologisesti aktiiviset kortikosteroidit ja ilmoittaa niiden toiminnot;
b) osoittavat, mikä kortikosteroidipuutos aiheuttaa hypoglukosemiaa ja lihasdystrofiaa tässä sairaudessa;
c) Nimeä ihon lisääntyneen pigmentaation syy Addisonin taudissa.
4. Potilaalle N, jolla oli kilpirauhasen vajaatoiminta, lääkäri määräsi hoidon, mukaan lukien tyroksiinin. 3 kuukautta hoidon aloittamisen jälkeen veren TSH-taso laski hieman. Miksi lääkäri suositteli tyroksiinin annoksen nostamista tälle potilaalle? Vastausta varten:
a) esittää kaavion muodossa kilpirauhashormonien synteesin ja erityksen säätelymekanismin;
5. Vuoristokylässä asuva 18-vuotias tyttö kääntyi endokrinologin puoleen valittaen yleisestä heikkoudesta, alentuneesta ruumiinlämpöstä ja mielialan heikkenemisestä. Potilas lähetettiin verikokeeseen TSH:n ja jodityroniinien varalta. Analyysin tulokset osoittivat TSH:n pitoisuuden nousun ja T4:n pitoisuuden laskun. Selittää:
a) mikä sairaus potilaalla voidaan olettaa;
b) mikä voi olla tällaisen patologian syy;
c) onko asuinpaikan ja tämän taudin esiintymisen välillä yhteyttä;
d) mitä ruokavaliota tulisi noudattaa tämän patologian estämiseksi;
e) jodityroniinien synteesin säätelykaavio ja verikokeen tulokset koehenkilöstä.
6. Diffuusi-toksisen struuman hoitoon käytetään tionamidiryhmän tyrostaattisia lääkkeitä (tiamatsoli). Tionamidien vaikutusmekanismi on, että kun ne tulevat kilpirauhaseen, ne estävät tyroperoksidaasin toimintaa. Selitä tionamidien terapeuttisen vaikutuksen tulos. Tätä varten:
a) nimeä tyrotoksikoosin tärkeimmät syyt ja kliiniset ilmenemismuodot;
b) antaa kaavio jodityroniinien synteesiä varten ja osoittaa vaiheet, joissa lääkkeet vaikuttavat;
c) osoittaa, miten jodityroniinien ja TSH:n pitoisuus muuttuu hoidon seurauksena;
d) Kuvaile aineenvaihdunnan muutoksia tionamidihoidon aikana.
Moduuliyksikkö 2 BIOKEMIALLISET MUUTOKSET AIHEUTTAMESSA PAASTON JA DIABEKETEEN AIKANA
Oppimistavoitteet Kykyä:
1. Tulkitse hiilihydraattien, rasvojen ja proteiinien aineenvaihdunnan muutoksia nälänhädän ja fyysisen rasituksen aikana kontrainsulaarihormonien vaikutuksesta.
2. Analysoi diabetes mellituksen syiden molekyylimekanismit.
3. Selitä diabeteksen oireiden ilmaantumisen mekanismeja aineenvaihduntaprosessien nopeuksien muutosten seurauksena.
4. Tulkitse paaston ja diabeteksen aineenvaihdunnan tärkeimmät erot.
Tietää:
1. Muutokset hormonaalisessa tilassa paaston aikana.
2. Muutos pääenergian kantajien vaihdossa nälänhädän aikana.
3. Muutokset hormonaalisessa tilassa ja energia-aineenvaihdunnassa diabetes mellituksessa.
4. Diabetes mellituksen pääoireet ja niiden esiintymismekanismit.
5. Diabeteksen akuuttien komplikaatioiden patogeneesi.
6. Diabetes mellituksen myöhäisten komplikaatioiden biokemiallinen perusta.
7. Diabetes mellituksen laboratoriodiagnoosin lähestymistavat.
8. Diabeteksen hoidon periaatteiden molekyylimekanismit ja lupaavat hoitosuunnat.
AIHE 11.6. MUUTOKSET HORMONAALISESSA TILASSA JA AIVANVAIHTOESSA PASOSTUN JA FYYLISEN TYÖN AIKANA
1. Imeytymisen jälkeisenä aikana ja paaston aikana veriplasman glukoositaso laskee normin alarajalle. Insuliini-glukagonisuhde pienenee. Näissä olosuhteissa syntyy tila, jolle on ominaista rasvojen, glykogeenin ja proteiinien hajoamisprosessien hallitseminen aineenvaihduntanopeuden yleisen laskun taustalla. Tänä aikana kontrainsulaaristen hormonien vaikutuksesta substraattien vaihto tapahtuu maksan, rasvakudoksen, lihasten ja aivojen välillä. Tällä vaihdolla on kaksi tarkoitusta:
Veren glukoosipitoisuuden ylläpitäminen glukoneogeneesin vuoksi glukoosiriippuvaisten kudosten (aivojen, punasolujen) aikaansaamiseksi;
Muiden "polttoaine"molekyylien, ensisijaisesti rasvojen, mobilisointi energian tuottamiseksi kaikille muille kudoksille.
Näiden muutosten ilmentymä antaa meille mahdollisuuden erottaa ehdollisesti kolme nälänhädän vaihetta. Johtuen aineenvaihdunnan siirtymisestä energian mobilisaatiotilaan, glukoosipitoisuus veressä on vähintään 65 mg/dl jopa 5-6 viikon paaston jälkeen. Tärkeimmät muutokset paaston aikana tapahtuvat maksassa, rasvakudoksessa ja lihaksissa (kuva 11.14).
2. Nälänhädän vaiheet. Nälkä se voi olla lyhytaikaista - päivän aikana (ensimmäinen vaihe), kestää viikon (toinen vaihe) tai useita viikkoja (kolmas vaihe).
AT ensimmäinen vaihe veren insuliinipitoisuus laskee noin 10-15 kertaa ruoansulatusjaksoon verrattuna ja glukagonin ja kortisolin pitoisuus kasvaa. Glykogeenivarastot ovat tyhjentyneet, rasvan mobilisoitumisnopeus ja glukoneogeneesin nopeus aminohapoista ja glyserolista lisääntyvät, veren glukoosipitoisuus laskee normin alarajalle (60 mg / dl).
 Riisi. 11.14. Muutokset pääenergian kantajien aineenvaihdunnassa paaston aikana:
Riisi. 11.14. Muutokset pääenergian kantajien aineenvaihdunnassa paaston aikana:
1 - insuliini-glukogonin indeksin lasku; 2 - glykogeenimobilisaatio; 3, 4 - GLA:n kuljetus aivoihin ja punasoluihin; 5 - TAG-mobilisointi; 6 - FA:n kuljetus lihaksiin; 7 - ketonikappaleiden synteesi; 8 - rasvahappojen kuljetus maksassa; 9 - AA:n kuljetus maksaan; 10 - glukoneogeneesi AA:sta; 11 - laktaatin kuljetus maksaan; 12 - glyserolin kuljetus maksaan. Pisteviiva osoittaa prosesseja, joiden nopeus laskee
Sisään toinen vaihe rasvojen mobilisaatio jatkuu, rasvahappojen pitoisuus veressä kasvaa, ketoaineiden muodostumisnopeus maksassa ja vastaavasti niiden pitoisuus veressä kasvaa; on asetonin hajua, joka vapautuu uloshengitetyn ilman ja hien mukana nälkäisestä henkilöstä. Glukoneogeneesi jatkuu kudosproteiinien hajoamisen kautta.
AT kolmas vaihe proteiinien hajoamisnopeus ja aminohappojen glukoneogeneesin nopeus laskevat. Aineenvaihdunta hidastuu. Typpitase on negatiivinen kaikissa nälänhädän vaiheissa. Ketonikappaleista tulee glukoosin ohella tärkeä energianlähde aivoille.
3. Muutokset pääenergian kantajien aineenvaihdunnassa nälänhädän aikana. Hiilihydraattien vaihto. Kehon glykogeenivarastot loppuvat 24 tunnin paaston aikana. Siten glykogeenin mobilisoitumisen ansiosta varmistetaan vain lyhytaikainen nälkä. Glukoneogeneesi on pääprosessi, joka tarjoaa kudoksille glukoosia paaston aikana. Glukoneogeneesi alkaa kiihtyä 4-6 tuntia viimeisen aterian jälkeen ja siitä tulee ainoa glukoosin lähde pitkäaikaisen paaston aikana. Glukoneogeneesin pääsubstraatit ovat aminohapot, glyseroli ja laktaatti.
4. Rasvojen ja ketoaineiden aineenvaihdunta. Ensimmäisten paastopäivien pääasiallinen energianlähde ovat rasvahapot, joita muodostuu rasvakudoksessa olevista TAG:eista. Ketonikappaleiden synteesi kiihtyy maksassa. Ketoniaineiden synteesi alkaa paaston ensimmäisinä päivinä. Ketonikappaleita käytetään pääasiassa lihaksissa. Myös aivojen energiantarpeet vastaavat osittain ketoaineista. Kolmen viikon paaston jälkeen lihaksissa olevien ketoaineiden hapettumisnopeus laskee ja lihakset käyttävät lähes yksinomaan rasvahappoja. Ketoniaineiden pitoisuus veressä kasvaa. Aivojen ketoaineiden käyttö jatkuu, mutta muuttuu vähemmän aktiiviseksi glukoneogeneesin ja glukoosipitoisuuden laskun vuoksi.
5. Proteiinin aineenvaihdunta. Ensimmäisten paastopäivien aikana lihasproteiinit hajoavat nopeasti - glukoneogeneesin tärkein substraattien lähde. Useiden viikkojen paaston jälkeen aminohappojen glukoneogeneesin nopeus laskee, mikä johtuu pääasiassa vähentyneestä glukoosin oton ja ketoaineiden käytön vähenemisestä aivoissa. Aminohapoista peräisin olevan glukoneogeneesin hidastuminen on välttämätöntä proteiinien säilymiselle, koska 1/3:n menetys kaikista proteiineista voi johtaa kuolemaan. Paaston kesto riippuu siitä, kuinka kauan ketoaineita voidaan syntetisoida ja käyttää. Oksaloasetaattia ja muita TCA-komponentteja tarvitaan kuitenkin ketonikappaleiden hapettumiseen. Normaalisti niitä muodostuu glukoosista ja aminohapoista, ja nälkäisenä vain aminohapoista.
AIHE 11.7. MUUTOKSET HORMONAALISESSA TILASSA JA aineenvaihdunnassa DIABETES MELLITUKSEESSA
1. Diabetes suhteellisen tai absoluuttisen insuliinin puutteen vuoksi. WHO:n luokituksen mukaan taudin kaksi päämuotoa erotetaan: tyypin I diabetes - insuliinista riippuvainen (IDDM), ja tyypin II diabetes (INSD)- insuliinista riippumaton.
2. IDSD on seurausta Langerhansin saarekkeiden β-solujen tuhoutumisesta autoimmuunireaktioiden seurauksena. Tyypin I diabetes voi johtua β-soluja tuhoavasta virusinfektiosta. Tällaisia viruksia ovat isorokko, vihurirokko, tuhkarokko, sytomegalovirus, sikotauti, Coxsackie-virus, adenovirus. IDDM aiheuttaa noin 25-30 % kaikista diabetestapauksista. Pääsääntöisesti β-solujen tuhoutuminen tapahtuu hitaasti, eikä taudin alkamiseen liity aineenvaihduntahäiriöitä. Kun 80-95 % soluista kuolee, ilmaantuu absoluuttinen insuliinin puutos ja kehittyy vakavia aineenvaihduntahäiriöitä. IDDM vaikuttaa useimpiin lapsiin, nuoriin ja nuoriin aikuisiin, mutta sitä voi esiintyä missä tahansa iässä (yhden vuoden iästä alkaen).
3. NIDSD kehittyy proinsuliinin insuliiniksi muuntumisen, insuliinin erityksen säätelyn, insuliinin katabolian lisääntymisen, insuliinisignaalin kohdesoluihin siirtymismekanismien vaurioitumisen seurauksena (esim. insuliinireseptori, insuliinisignaalin solunsisäisten välittäjien vaurioituminen jne.), insuliinireseptoreiden vasta-aineiden muodostuminen ja insuliinin pitoisuus veressä voi olla normaalia tai jopa kohonnutta. Taudin kehittymisen ja kliinisen kulun määrääviä tekijöitä ovat liikalihavuus, huono ruokavalio, istuvat elämäntavat ja stressi. NIDDM vaikuttaa ihmisiin, yleensä yli 40-vuotiaisiin, kehittyy vähitellen, oireet ovat lieviä. Akuutit komplikaatiot ovat harvinaisia.
4. Metaboliset muutokset diabetes mellituksessa. Diabetes mellituksessa insuliinin ja glukagonin suhde yleensä pienenee. Tämä heikentää glykogeenin ja rasvojen kertymisen stimulaatiota ja lisää energiavarastojen mobilisaatiota. Maksa, lihakset ja rasvakudos toimivat myös syömisen jälkeen imeytymisen jälkeisessä tilassa.
5. Diabeteksen oireet. Hyperglukosemia. Kaikille diabeteksen muodoille on ominaista kohonnut veren glukoosipitoisuus. hyperglukosemia, sekä aterioiden jälkeen että tyhjään mahaan, sekä glukosuria. Aterian jälkeen glukoosipitoisuus voi nousta 300-500 mg/dl ja pysyy korkealla imeytymisen jälkeisenä aikana, ts. heikentynyt glukoositoleranssi.
Glukoositoleranssin laskua havaitaan myös diabeteksen piilevän (latentin) muodon tapauksissa. Näissä tapauksissa ihmisillä ei ole diabetes mellitukselle tyypillisiä valituksia ja kliinisiä oireita, ja tyhjän mahan veren glukoosipitoisuus vastaa normaalin ylärajaa. Provokatiivisten testien käyttö (esimerkiksi sokerikuorma) paljastaa kuitenkin glukoosinsietokyvyn heikkenemisen (kuva 11.15).
IDDM:n glukoosipitoisuuden nousu veriplasmassa johtuu useista syistä. Insuliini-glukagoniindeksin pienentyessä kontrainsulaaristen hormonien vaikutukset lisääntyvät, glukoosin kantajaproteiinien (GLUT-4) määrä insuliiniriippuvaisten solujen kalvoilla (rasvakudos ja lihakset) vähenee. Tämän seurauksena näiden solujen glukoosin kulutus vähenee. Lihaksiin ja maksaan glukoosi ei kerrostu glykogeenin muodossa, rasvakudoksessa rasvan synteesi- ja kerrostumisnopeus laskee. Lisäksi konrinsulaaristen hormonien, pääasiassa glukagonin, toiminta aktivoi glukoneogeneesiä aminohapoista, glyserolista ja laktaatista. Veren glukoosipitoisuuden nousu diabetes mellituksessa yli munuaispitoisuuden kynnyksen 180 mg/dl aiheuttaa glukoosin erittymisen virtsaan.
Ketonemia on tyypillinen diabeteksen oire. Insuliinin ja glukagonin alhaisella suhteella rasvat eivät kerrostu, niiden katabolia kiihtyy, koska hormoniherkkä lipaasi rasvakudoksessa on fosforyloidussa aktiivisessa muodossa. Esteröimättömien rasvahappojen pitoisuus veressä kasvaa. Maksa imee rasvahapot ja hapettaa ne asetyyli-CoA:ksi, joka puolestaan
 Riisi. 11.15. Muutokset glukoosin sietokyvyssä potilailla, joilla on piilevä diabetes mellitus.
Riisi. 11.15. Muutokset glukoosin sietokyvyssä potilailla, joilla on piilevä diabetes mellitus.
Glukoositoleranssin määritystä käytetään diabetes mellituksen diagnosoinnissa. Potilas ottaa glukoosiliuosta 1 g per 1 kg ruumiinpainoa (sokerikuorma). Veren glukoosipitoisuus mitataan 2-3 tunnin sisällä 30 minuutin välein. 1 - terveellä henkilöllä, 2 - potilaalla, jolla on diabetes mellitus
muuttuu β-hydroksivoi- ja asetoetikkahapoiksi, mikä lisää ketoaineiden pitoisuutta veressä - ketonemia. Kudoksissa asetoasetaatti dekarboksyloituu osittain asetoniksi, jonka haju tulee diabeetikoista ja tuntuu kaukaakin. Ketoniaineiden pitoisuuden nousu veressä (yli 20 mg/dl, joskus jopa 100 mg/dl) johtaa ketonuria. Ketoniaineiden kerääntyminen heikentää veren puskurointikykyä ja aiheuttaa asidoosi (ketoasidoosi).
Hyperlipoproteinemia. Ruokavalion rasvat eivät kerrostu rasvakudokseen varastointiprosessien heikkenemisen ja Lp-lipaasin alhaisen aktiivisuuden vuoksi, vaan ne kulkeutuvat maksaan, jossa ne muuttuvat triasyyliglyseroleiksi, jotka kulkeutuvat maksasta osana VLDL:ää.
Azotemia. Diabetes insuliinin puutos johtaa synteesinopeuden hidastumiseen ja proteiinien hajoamisen lisääntymiseen kehossa. Tämä lisää aminohappojen pitoisuutta veressä. Aminohapot kulkeutuvat maksaan ja deaminoituvat. Glykogeenisten aminohappojen typettömät tähteet sisältyvät glukoneogeneesiin, mikä lisää edelleen hyperglykemiaa. Tuloksena oleva ammoniakki siirtyy ornitiinikiertoon, mikä johtaa urean pitoisuuden nousuun veressä ja vastaavasti virtsassa - atsotemia ja atsoturia.
Polyuria. Suuri määrä nestettä tarvitaan poistamaan suuria määriä glukoosia, ketoaineita ja ureaa, mikä voi johtaa kuivumiseen. Tämä johtuu munuaisten keskittymiskyvyn erityispiirteistä. Esimerkiksi potilaiden virtsan eritys lisääntyy useita kertoja ja saavuttaa joissakin tapauksissa 8-9 litraa päivässä, mutta useammin se ei ylitä 3-4 litraa. Tätä oiretta kutsutaan polyuria. Veden menetys aiheuttaa jatkuvaa janoa ja lisääntynyttä vedenottoa - polydipsia.
6. Diabeteksen akuutit komplikaatiot. Diabeettisen kooman kehittymismekanismit. Diabetes mellituksen hiilihydraattien, rasvojen ja proteiinien aineenvaihdunnan häiriöt voivat johtaa kooman (akuutien komplikaatioiden) kehittymiseen. Diabeettinen kooma ilmenee kaikkien kehon toimintojen jyrkänä rikkomisena, johon liittyy tajunnan menetys. Diabeettisen kooman tärkeimmät esiasteet ovat asidoosi ja kudosten kuivuminen (kuva 11.16).
Diabeteksen dekompensoituessa vesi- ja elektrolyyttiaineenvaihdunnassa kehittyy häiriöitä. Syynä tähän on hyperglukosemia, johon liittyy osmoottisen paineen nousu verisuonikerroksessa. Osmolaarisuuden ylläpitämiseksi alkaa nesteen kompensoiva liike soluista ja solunulkoisesta tilasta verisuonikerrokseen. Tämä johtaa kudosten veden ja elektrolyyttien, pääasiassa Na+-, K+-, Cl-, HCO 3 --ionien, katoamiseen. Seurauksena kehittyy vakava soludehydraatio ja solunsisäisten ionien (ensisijaisesti K+) puutos, johon liittyy yleinen dehydraatio. Tämä johtaa perifeerisen verenkierron heikkenemiseen, aivojen ja munuaisten verenkierron vähenemiseen ja hypoksiaan. Diabeettinen kooma kehittyy hitaasti useiden päivien aikana, mutta voi joskus
 Riisi. 11.16. Diabetes mellituksen metaboliset muutokset ja diabeettisen kooman syyt
Riisi. 11.16. Diabetes mellituksen metaboliset muutokset ja diabeettisen kooman syyt
tapahtuu muutaman tunnin sisällä. Ensimmäiset merkit voivat olla pahoinvointi, oksentelu, letargia. Potilaiden valtimopaine on alentunut.
Diabetes mellituksen kooma voi ilmetä kolmessa päämuodossa: ketoasidoottinen, hyperosmolaarinen ja maitohappoasidoottinen.
Ketoasidoottiselle koomalle on ominaista vakava insuliinin puute, ketoasidoosi, polyuria ja polydipsia. Insuliinin puutteen aiheuttamaan hyperglukosemiaan (20-30 mmol / l) liittyy suuria neste- ja elektrolyyttihäviöitä, kuivumista ja plasman hyperosmolaarisuutta. Ketonikappaleiden kokonaispitoisuus saavuttaa 100 mg / dl ja enemmän.
klo hyperosmolaarinen koomassa on aina erittäin korkea plasman glukoositaso, polyuria, polydipsia ja vaikea kuivuminen. Uskotaan, että useimmilla potilailla hyperglukosemia johtuu samanaikaisesta munuaisten vajaatoiminnasta. Seerumin ketoaineita ei yleensä havaita.
klo maitohappohappoinen koomassa hypotensio, perifeerisen verenkierron heikkeneminen ja kudosten hypoksia ovat vallitsevia, mikä johtaa aineenvaihdunnan siirtymiseen kohti anaerobista glykolyysiä, mikä aiheuttaa maitohapon pitoisuuden nousua veressä (maitohappoasidoosi).
7. Diabeteksen myöhäiset komplikaatiot ovat seurausta pitkittyneestä hyperglukosemiasta ja johtavat usein potilaiden varhaiseen vammautumiseen. Hyperglukosemia johtaa verisuonten vaurioitumiseen ja eri kudosten ja elinten toimintahäiriöihin. Yksi tärkeimmistä kudosvaurion mekanismeista diabetes mellituksessa on glukosylaatio proteiinit ja niihin liittyvät kudossolujen toimintahäiriöt, muutokset veren reologisissa ominaisuuksissa ja hemodynamiikassa (juoksevuus, viskositeetti).
Jotkut yhdisteet sisältävät normaalisti hiilihydraattikomponentteja (glykoproteiineja, proteoglykaaneja, glykolipidejä). Näiden yhdisteiden synteesi tapahtuu entsymaattisten reaktioiden (entsymaattinen glukosylaatio) seurauksena. Glukoosin aldehydiryhmän ei-entsymaattista vuorovaikutusta proteiinien vapaiden aminoryhmien kanssa (ei-entsymaattinen glukosylaatio) voi kuitenkin tapahtua myös ihmiskehossa. Terveiden ihmisten kudoksissa tämä prosessi on hidasta ja kiihtyy hyperglukosemiassa.
Yksi ensimmäisistä diabeteksen oireista on glukosyloidun hemoglobiinin 2-3-kertainen nousu. Koko erytrosyyttien elinkaaren ajan glukoosi tunkeutuu vapaasti sen kalvon läpi ja sitoutuu peruuttamattomasti hemoglobiiniin ilman entsyymien osallistumista pääasiassa β-ketjujen kautta. Tässä tapauksessa muodostuu hemoglobiinin HbA 1c glukosyloitu muoto. Tätä hemoglobiinin muotoa on pieninä määrinä terveillä ihmisillä. Kroonisessa hyperglukosemiassa HbA 1c:n prosenttiosuus hemoglobiinin kokonaismäärästä kasvaa.
Proteiinin glukosylaatioaste riippuu niiden uusiutumisnopeudesta. Hitaasti metaboloituviin proteiineihin kertyy enemmän muutoksia. Hitaasti vaihtuviin proteiineihin kuuluvat solujen väliset proteiinit
matriisi, tyvikalvot, silmän linssi (kiteet). Pohjakalvojen paksuuntuminen on yksi varhaisista ja pysyvistä diabeteksen oireista, joka ilmenee diabeettisena angiopatiana.
Muutoksia, jotka ilmenevät valtimoiden elastisuuden heikkenemisenä, aivojen, sydämen ja alaraajojen suurten ja keskisuurten verisuonten vaurioitumisesta, kutsutaan diabeettiset makroangiopatiat. Ne kehittyvät solujen välisen matriksin proteiinien - kollageenin ja elastiinin - glukosylaation seurauksena, mikä johtaa verisuonten elastisuuden vähenemiseen ja verenkierron heikkenemiseen.
Hiussuonien ja pienten alusten vaurioiden tulos - m ikroangiopatia ilmenee nefro- ja retinopatiana. Joidenkin diabetes mellituksen myöhäisten komplikaatioiden (kaihi, retinopatia) syy voi olla glukoosin sorbitoliksi muuntumisnopeuden lisääntyminen. Sorbitolia ei käytetä muissa aineenvaihduntareiteissä, ja sen diffuusionopeus soluista on alhainen. Diabetes mellituspotilailla sorbitoli kerääntyy verkkokalvoon ja silmän linssiin, munuaisten glomerulussoluihin, Schwann-soluihin ja endoteeliin. Sorbitoli on myrkyllistä soluille korkeina pitoisuuksina. Sen kerääntyminen hermosoluihin johtaa osmoottisen paineen nousuun, solujen turvotukseen ja kudosturvotukseen. Linssin samentumista tai kaihia voi kehittyä sekä sorbitolin kertymisen ja kristalliinien järjestyneen rakenteen häiriintymisen aiheuttaman linssin turpoamisen seurauksena että kristalliinien glukosyloitumisesta, jotka muodostavat monimolekyylisiä aggregaatteja, jotka lisäävät linssin taittovoimaa. linssi.
TEHTÄVÄT OPIN ULKOPUOLISTA TYÖTÄ
1. Harkitse kuvaa. 11.14, piirrä kaavioita maksassa ja muissa kudoksissa postabsorptiojakson aikana kiihtyneistä prosesseista, kirjoita muistiin aineenvaihduntareittien nimet ja vastaavat säätelyentsyymit.
2. Analysoi aineenvaihdunnan muutokset, jotka näkyvät kuvassa. 11.10 ja 11.11 ja vertaa niitä kuvassa esitettyihin muutoksiin. 11.14. Tätä varten:
a) nimeä prosessit, jotka aktivoituvat ja estyvät pitkäaikaisen nälänhädän aikana;
b) valita ja kirjoittaa prosessikaaviot, joiden ansiosta veren glukoosipitoisuus säilyy pitkäaikaisen paaston aikana;
c) ilmoittaa kullekin valitulle prosessille tärkeimmät entsyymit ja
munkit, joiden vaikutuksen alaisena he aktivoituvat;
d) valita ja kirjoittaa prosessien kaaviot, joiden vuoksi se suorittaa -
Xia lihasten energian saanti pitkäaikaisen nälänhädän aikana.
3. Tarkastele kaaviota diabetes mellituksen metabolisista muutoksista (Kuva 11.16) Selitä hyperglukosemian syyt Kirjoita muistiin näissä olosuhteissa kiihtyvien aineenvaihduntareittien nimet.
4. Selitä ketoasidoosin syyt ja mekanismit diabetes mellituksessa ja piirrä vastaava kaavio.
5. Vertaa hormonaalisen tilan ja aineenvaihdunnan muutoksia diabeteksessa ja paastossa (kuvat 11.14 ja 11.16). Selitä, miksi rasvojen ja proteiinien hajoaminen tapahtuu diabetes mellituksen hyperglykemian taustalla.
6. Luettele diabeteksen tärkeimmät oireet. Perustele lauseen pätevyys: "diabetes on nälkää runsauden keskellä." Tätä varten:
a) nimeä diabetes mellituksen ilmenemismuotoja, jotka ovat samanlaisia kuin nälänhädän aikana tapahtuvat aineenvaihdunnan muutokset;
b) selittää näiden muutosten syyt;
c) nimeä tärkeimmät aineenvaihdunnan erot diabeteksessa ja nälkään.
7. Jatka diabeteksen myöhäisten komplikaatioiden taulukon täyttämistä (taulukko 11.2):
Taulukko 11.2. Diabeteksen myöhäiset komplikaatiot
ITSEHALLINTA TEHTÄVÄT
1. Valitse oikea vastaus.
Paaston aikana:
A. Asetyyli-CoA-karboksylaasi on fosforyloitunut ja aktiivinen B. Hormoniherkkä TAG-lipaasi on inaktiivinen
B. Lp-lipaasi on aktiivinen rasvakudoksessa
D. Maksan pyruvaattikinaasi on fosforyloitunut ja aktiivinen E. cAMP-riippuvainen proteiinikinaasi on aktiivinen adiposyyteissä
2. Valitse oikeat vastaukset. Kolmen päivän paaston kanssa:
A. Insuliini-glukagoni-indeksi pienenee
B. Aminohapojen glukoneogeneesin nopeus kasvaa
B. TAG-synteesin nopeus maksassa laskee D. β-hapetuksen nopeus maksassa laskee
D. Ketoniaineiden pitoisuus veressä on normaalia korkeampi
3. Valitse oikeat vastaukset.
Ketonikappaleiden synteesin lisääntyminen nälän aikana johtuu seuraavista:
A. Vähentyneet glukagonitasot
B. Vähentynyt asetyyli-CoA:n muodostuminen maksassa
B. Rasvahappojen pitoisuuden lisääminen veriplasmassa D. β-hapetusnopeuden vähentäminen maksassa
E. Hormoniherkän TAG-lipaasin vähentynyt aktiivisuus adiposyyteissä
4. Valitse oikeat vastaukset.
Diabetes mellituksessa maksa:
A. Glykogeenisynteesin kiihtyminen
B. Glukoneogeneesin nopeuden nousu
B. Rasvan synteesin hidastunut nopeus
D. Asetaoasetaatin synteesin nopeuden lisääminen
D. Asetyyli-CoA-karboksylaasin lisääntynyt aktiivisuus
5. Aseta ottelu:
A. Korkea insuliinitaso B. Alkaloosi
B. Hypoglukosemia
D. Korkeat kortisolitasot
E. Autoimmuunivaurio β-soluille
1. Vain diabeteksen kanssa
2. Vain paaston aikana
3. Vain steroididiabetes
6. Valitse oikeat vastaukset.
IDDM-potilaat löytävät useimmiten:
A. Hyperglukosemia
B. Korkea insuliinikatabolian nopeus
B. Insuliinipitoisuus veressä on normaali tai sen yläpuolella. D. Vasta-aineet haiman β-soluille
D. Mikroangiopatia
7. Aseta ottelu:
A. Makroangiopatia B. Kaihi
B. Mikroangiopatia D. Nefropatia
D. Neuropatia
1. Sorbitolireitin aktivointi Schwann-soluissa
2. Kristalliinien glukosylaatio
3. Munuaisten glomerulusten tyvikalvojen paksuuntuminen
VASTAUKSIEN STANDARDIT "ITSEENHALLINTA TEHTÄVÄT"
2. A, B, C, D
4. B, C, D
5. 1-D, 2-B, 3-G
6. A, G, D
7. 1-D, 2-B, 3-D
PERUSKÄSITTEET JA KÄSITTEET
1. Paasto
2. Paastovaiheet
3. Diabetes
6. Hyperglukosemia - glukosuria
7. Ketonemia - ketonuria
8. Atsotemia - atsoturia
9. Diabeteksen myöhäiset komplikaatiot
10. Diabeettinen kooma
11. Ketoasidoottinen kooma
12. Hyperosmolaarinen kooma
13. Maitohappokooma
14. Mikroangiopatia
15. Makroangiopatia
16. Neuropatia
17. Nefropatia
TEHTÄVÄT KUULUTUSTYÖHÄN
Ratkaista ongelmia
1. Turistit eivät laskeneet ruokavarastoja, ja ennen kuin he saavuttivat ensimmäisen asutuksen, heidät pakotettiin näkemään nälkää 2 päivää. Mitä muutoksia näiden matkailijoiden aineenvaihdunnassa tapahtuu? Selitykseksi:
a) ilmoittaa, kuinka glukoosipitoisuus turistien veressä muuttuu toisen paastopäivän loppuun mennessä;
b) kirjoittaa prosessien kaaviot, joiden aktivoitumisen ansiosta normaali glukoosipitoisuus säilyy ensimmäisenä paastopäivänä;
c) nimeä hormonit, jotka säätelevät glukoositasoa tänä aikana;
d) esittää kaavion muodossa näiden hormonien vaikutusmekanismit;
e) ilmoittaa näiden reittien säätelyreaktiot ja niiden aktivointitavat.
2. Biokemialliset tutkimukset tyypin 1 diabetes mellitusta sairastavan potilaan verestä ja virtsasta osoittivat:
Miten nämä indikaattorit muuttuvat, kun potilaalle annetaan keskimääräinen päivittäinen insuliiniannos? Mitä prosessien aktivoinnin seurauksena nämä muutokset tapahtuvat?
3. Potilas tuli terapeutille valittaen etenevää heikkoutta, uneliaisuutta, huimausta. Paasto pahensi oireita, mikä sai lääkärin olettamaan, että potilaalla oli hypoglykemia. Verikoe vahvisti oletuksen (glukoositaso alle 2,5 mmol/l) ja osoitti myös voimakkaasti kohonnutta C-peptidipitoisuutta (yli 800 pmol/l). Potilas ei sairasta diabetesta eikä käytä sokeria alentavia lääkkeitä. Mitä sairautta voidaan olettaa? Kun vastaat kysymykseen:
a) nimeä ärsykkeet, jotka vaikuttavat insuliinin eritykseen;
b) kuvaa insuliinin vaikutusta hiilihydraatti- ja rasva-aineenvaihduntaan maksassa, rasvakudoksessa ja lihaksissa;
c) selittää, miksi hypoglukosemia on vaarallista ja mitkä prosessit kehossa normaalisti estävät hypoglukosemian kehittymisen jopa nälänhädän aikana;
d) nimeä sairaus ja ehdota hoitomenetelmää.
4. Potilas N valitti jatkuvaa nälkää, janoa, väsymystä ja uupumusta. Paastoglukoosipitoisuuden määritys osoitti 130 mg/dl. Mitä lisätutkimuksia diagnoosin vahvistamiseksi tulisi tehdä tässä tapauksessa? Mitä tuloksia voidaan ennustaa, jos tutkittavalla todetaan tyypin II diabetes?
5. Potilas, jolla on diagnosoitu IDDM, ei ole saanut insuliinia pitkään aikaan. Kun potilas meni lääkäriin ja perusteellisen tutkimuksen, hänelle määrättiin insuliinihoito. Kahden kuukauden kuluttua paastoveren glukoosipitoisuuden määritys osoitti 85 mg / dl, glukosyloidun hemoglobiinin taso oli 14 % hemoglobiinin kokonaistasosta (normaali 5,8-7,2 %).
Mitkä ovat mahdolliset syyt korkeaan glukosyloidun hemoglobiinin pitoisuuteen tällä potilaalla jatkuvasta hoidosta huolimatta? Anna esimerkkejä muiden proteiinien glukosylaatiosta. Selitä, mihin komplikaatioihin tämä voi johtaa.
6. 39-vuotias potilas otettiin hoitoon ja valittivat voimakasta janoa ja nopeaa väsymystä. Painonpudotus viimeisen 5 viikon aikana oli 4 kg hyvästä ruokahalusta ja normaalista liikunnasta huolimatta. Verikoe osoitti, että glukoosipitoisuus 2 tuntia aterian jälkeen on 242 mg / dl. Mitä sairautta tällä potilaalla voidaan olettaa? Mikä on janon syy? Miten selittää potilaan nopea väsymys?
Modulaarinen yksikkö 3 VESI-SUOLAILAN SÄÄTELY. VASOPRESSIININ, ALDOSTERONIN JA RENINI-ANGIOTENSIINIJÄRJESTELMÄN ROOLI. CA 2+ - JA FOSFAATTIAINEENAAN SÄÄTELY
Oppimistavoitteet Kykyä:
1. Analysoi aineenvaihdunnan muutoksia, joita esiintyy joissakin vesi-suola-aineenvaihdunnan häiriöissä (hyperaldosteronismi, munuaisten verenpainetauti).
2. Selvitä kalsiumaineenvaihduntaa säätelevien hormonien synteesin ja erittymisen häiriöiden molekyylimekanismit.
Tietää:
1. WOS:n päähormonien ominaisuudet ja sen säätelyn vaiheet.
2. Kalsiumin päätehtävät elimistössä.
3. Kalsium- ja fosfaatti-ionien vaihdon hormonaalisen säätelyn mekanismit.
4. Ilmeiset eräät kalsiumin ja fosfaattien vaihtoa säätelevien hormonien synteesin ja erityksen häiriöt (hypo- ja hyperparatyreoosi, riisitauti).
AIHE 11.8. VESI-SUOLAIDEN SÄÄTELY
1. Pääparametrit vesi-suolan homeostaasi ovat osmoottinen paine, pH ja solunsisäisen ja ekstrasellulaarisen nesteen tilavuus. Muutokset näissä parametreissa voivat johtaa verenpaineen muutoksiin, asidoosiin tai alkaloosiin, kuivumiseen ja turvotukseen. Tärkeimmät vesi-suolatasapainon säätelyyn osallistuvat hormonit ovat antidiureettinen hormoni (ADH), aldosteroni ja eteisen natriureettinen tekijä (ANF).
2. Antidiureettinen hormoni(ADH) tai vasopressiini on peptidi, joka sisältää yhdeksän aminohappoa, jotka on yhdistetty yhdellä disulfidisillalla. Se syntetisoidaan prohormonina hypotalamuksessa, siirretään sitten aivolisäkkeen takaosan hermopäätteisiin, joista se erittyy verenkiertoon asianmukaisella stimulaatiolla. Liikkuminen aksonia pitkin liittyy tiettyyn kantajaproteiiniin (neurofysiini) (kuva 11.17).
ADH:n erittymistä aiheuttava ärsyke on natrium-ionien pitoisuuden nousu ja solunulkoisen nesteen osmoottisen paineen nousu.
ADH:n tärkeimmät kohdesolut ovat distaalisten tubulusten solut ja munuaisten keräyskanavat. Näiden kanavien solut ovat suhteellisen vettä läpäisemättömiä, ja ADH:n puuttuessa virtsa ei tiivisty ja sitä voi erittyä yli 20 litraa päivässä (normaalisti 1-1,5 litraa päivässä).
 Riisi. 11.17. Antidiureettisen hormonin eritys ja vaikutusmekanismi:
Riisi. 11.17. Antidiureettisen hormonin eritys ja vaikutusmekanismi:
A: 1 - supraoptinen neuroni; 2 - paraventrikulaarinen neuroni; 3 - aivolisäkkeen etulohko; 4 - aivolisäkkeen takalohko; 5 - ADH-neurofysiini; B: 1 - ADH sitoutuu kalvoreseptoriin V2 aiheuttaen adenylaattisyklaasin (AC) aktivoitumisen ja sen seurauksena cAMP:n muodostumisen; 2 - cAMP aktivoi proteiinikinaasia, joka fosforyloi proteiineja; 3 - fosforyloidut proteiinit indusoivat akvaporiiniproteiinigeenin transkription; 4 - akvaporiini on upotettu munuaistiehyen solukalvoon
ADH:lle on olemassa kahden tyyppisiä reseptoreita - V1 ja V2. V2-reseptori löytyy vain munuaisten epiteelisolujen pinnalta. ADH:n sitoutuminen V2:een liittyy adenylaattisyklaasijärjestelmään ja stimuloi proteiinikinaasin (PKA) aktivaatiota. Proteiinikinaasi fosforyloi proteiineja, jotka stimuloivat kalvoproteiinigeenin, akvaporiini-2:n, ilmentymistä. Aquaporin-2 siirtyy apikaaliselle kalvolle, integroituu siihen ja muodostaa vesikanavia, joiden kautta vesimolekyylit diffundoituvat vapaasti soluihin
munuaistiehyissä ja sitten interstitiaaliseen tilaan. Tämän seurauksena vesi imeytyy takaisin munuaistiehyistä (katso kuva 11.17). Tyypin V reseptorit lokalisoituu sileän lihaksen kalvoihin. ADH:n vuorovaikutus V1-reseptorin kanssa johtaa fosfolipaasi C:n aktivoitumiseen, mikä johtaa Ca2+:n vapautumiseen endoplasmisesta retikulumista ja verisuonten sileän lihaskerroksen supistumisesta.
3. Diabetes insipidus. ADH-puutos, joka johtuu aivolisäkkeen takaosan toimintahäiriöstä sekä hormonaalisen signaalinsiirtojärjestelmän häiriö, voi johtaa kehitykseen. diabetes insipidus. Diabetes insipiduksen pääasiallinen ilmentymä on polyuria, nuo. suurien määrien matalatiheyksisen virtsan erittyminen.
4. Aldosteroni- aktiivisin mineralokortikosteroidi - syntetisoivat lisämunuaiskuoren glomerulaarivyöhykkeen solut kolesterolista. Aldosteronin synteesiä ja eritystä stimuloivat alhainen Na + -pitoisuus, korkea K + -pitoisuus ja reniini-angiotensiinijärjestelmä. Hormoni tunkeutuu munuaistiehyiden soluihin, on vuorovaikutuksessa tietyn sytoplasmisen tai tuman reseptorin kanssa (kuva 11.18) ja indusoi proteiinien synteesiä, jotka tarjoavat natriumionien uudelleenabsorption ja kaliumionien erittymisen.
Lisäksi proteiinit, joiden synteesi on aldosteronin indusoima, lisäävät Na +, K + -ATPaasipumppujen määrää ja toimivat myös TCA:n entsyymeinä tuottaen ATP-molekyylejä aktiiviseen ionikuljetukseen. Aldosteronin toiminnan kokonaistulos on NaCl:n pysyminen kehossa.
5. Päärooli vesi-suola-tasapainon säätelyssä ja siten veren tilavuuden ja verenpaineen säätelyssä on järjestelmällä. reniini-angiotensiini-aldosteroni(Kuva 11.19).
proteolyyttinen entsyymi reniini Munuaisten afferenttien arteriolien juxtaglomerulaariset solut syntetisoivat. Verenpaineen lasku afferenteissa arterioleissa, nesteen tai veren menetys ja NaCl-pitoisuuden lasku stimuloivat reniinin vapautumista. maksassa tuotettu proteiini angiotensinogeeni reniini hydrolysoi muodostaen angiotensiini I:n, joka puolestaan toimii substraattina ACE:lle (angiotensiinia konvertoiva entsyymi karboksidipentidyylipeptidaasi). Dipeptidi lohkeaa angiotensiini I:stä angiotensiini II:n muodostamiseksi. Inositolifosfaattijärjestelmän kautta giotensiini II stimuloi aldosteronin synteesiä ja eritystä. Koska angiotensiini II on myös voimakas verisuonia supistava aine, se aiheuttaa verisuonten sileälihassolujen supistumista, vastaavasti verenpaineen nousua ja lisäksi janoa.
6. Reniini-angiotensiini-aldosteronijärjestelmä tarjoaa veren tilavuuden palauttaminen, joka voi pienentyä verenvuodon, runsaan oksentelun, ripulin, hikoilun seurauksena - tilat, jotka ovat merkki
 Riisi. 11.18. Aldosteronin vaikutusmekanismi.
Riisi. 11.18. Aldosteronin vaikutusmekanismi.
Aldosteroni, joka on vuorovaikutuksessa solunsisäisten reseptorien kanssa, stimuloi proteiinisynteesiä. Nämä proteiinit voivat olla:
1 - natriumkanavien komponentit ja lisäävät Na +:n reabsorptiota virtsasta;
2 - TCA-entsyymit, joiden aktiivisuus varmistaa ATP:n tuotannon; 3 - Na +, K + -ATPaasi, pumppu, joka ylläpitää matalaa solunsisäistä natriumionipitoisuutta ja korkeaa kaliumionipitoisuutta
reniinin vapautuminen. Tätä helpottaa myös eteisten ja valtimoiden baroreseptoreista tulevien impulssien väheneminen nesteen suonensisäisen tilavuuden pienenemisen seurauksena. Tämän seurauksena angiotensiini II:n muodostuminen lisääntyy ja vastaavasti aldosteronin pitoisuus veressä kasvaa, mikä aiheuttaa natriumionien pidättymistä. Tämä viestii hypotalamuksen osmoreseptoreista ja ADH:n erityksestä aivolisäkkeen etummaisista hermopäätteistä, mikä stimuloi veden takaisinimeytymistä keräyskanavista. Angiotensiini II, jolla on voimakas vasokonstriktiivinen vaikutus, nostaa verenpainetta ja lisää myös janoa. Juomisen mukana tuleva vesi jää elimistössä normaalia suuremmassa määrin.
 Riisi. 11.19. Reniini-angiotensiini-aldosteronijärjestelmä.
Riisi. 11.19. Reniini-angiotensiini-aldosteronijärjestelmä.
ACE - angiotensiiniä konvertoiva entsyymi (toinen nimie)
Vähentynyt nestetilavuus ja alentunut verenpaine aktivoivat reniini-angiotensiini-aldosteronijärjestelmän;
Angiotensiini II aiheuttaa ohimenevää vasokonstriktiota ja verenpaineen nousua;
Aldosteroni stimuloi natriumin retentiota, mikä johtaa vasopressiinin vapautumiseen ja lisääntyneeseen veden takaisinimeytymiseen;
Angiotensiini II aiheuttaa myös janon tunnetta, mikä lisää nesteen määrää kehossa.
Nestetilavuuden kasvu ja verenpaineen nousu johtavat reniini-angiotensiinijärjestelmän aktivoitumisen ja aldosteronin erittymisen aiheuttaneen ärsykkeen eliminoitumiseen, ja seurauksena on veren tilavuuden palautuminen.
7. Perfuusiopaineen lasku munuaiskeräsissä voi myös johtua munuaisvaltimon kaventumisesta (stenoosista) tai nefroskleroosista. Tässä tapauksessa myös koko reniini-angiotensiinijärjestelmä kytkeytyy päälle. Mutta koska alkutilavuus ja verenpaine ovat normaalit, järjestelmän sisällyttäminen johtaa verenpaineen nousuun normin yläpuolelle ja ns. munuaisten hypertensio.
8. Hyperaldosteronismi - on sairaus, jonka aiheuttaa lisämunuaisten aldosteronin liikaeritys. Syy primaarinen hyperaldosteronismi (Kohnin oireyhtymä) on lisämunuaisten adenooma tai aldosteronia tuottavien glomerulaarivyöhykkeen solujen diffuusi hypertrofia. Primaarisessa hyperaldosteronismissa ylimääräinen aldosteroni lisää natriumin takaisinabsorptiota munuaistiehyissä. Plasman Na + -pitoisuuden kasvu stimuloi antidiureettisen hormonin eritystä ja vedenpidätystä munuaisissa. Lisäksi kalium-, magnesium- ja protoni-ionien erittyminen tehostuu. Tämän seurauksena kehittyy hypernatremia, joka aiheuttaa erityisesti kohonnutta verenpainetta, hypervolemiaa ja turvotusta; hypokalemia, joka johtaa lihasheikkouteen, sekä magnesiumin puutos ja metabolinen alkaloosi. Syy sekundaarinen hyperaldosteronismi on kohonnut reniinin ja angiotensiini II:n taso, se stimuloi lisämunuaiskuorta ja johtaa liialliseen aldosteronin synteesiin. Kliiniset oireet ovat vähemmän ilmeisiä kuin primaarisessa aldosteronismissa. Aldosteronipitoisuuden ja plasman reniiniaktiivisuuden samanaikainen määritys mahdollistaa primaarisen (plasman reniiniaktiivisuuden väheneminen) ja sekundaarisen (plasman reniiniaktiivisuuden lisääntymisen) hyperaldosteronismin erottamisen.
9. Eteisen natriureettinen tekijä (ANF)- peptidi, joka syntetisoidaan ja varastoituu prohormonina sydänsoluissa. Pääasiallinen PNP:n eritystä säätelevä tekijä on verenpaineen nousu. PNP:n tärkeimmät kohdesolut ovat munuaiset, lisämunuaiset ja ääreisvaltimot. Plasmakalvon PNP-reseptori on katalyyttinen reseptori, jolla on. Tuloksena
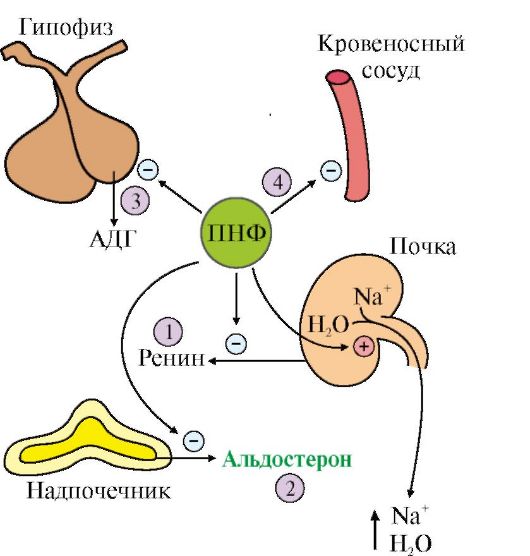 Riisi. 11.20. PNF-toiminnan vaikutukset:
Riisi. 11.20. PNF-toiminnan vaikutukset:
1 - estää reniinin vapautumista; 2 - estää aldosteronin eritystä; 3 - estää ADH:n eritystä; 4 - aiheuttaa verisuonten rentoutumista
Kun PNP sitoutuu reseptoriin, reseptorin guanylaattisyklaasiaktiivisuus lisääntyy ja GTP:stä muodostuu syklistä GMP:tä. PNP:n toiminnan seurauksena reniinin ja aldosteronin muodostuminen ja erittyminen estyy. PNP:n nettovaikutus on lisätä Na +:n ja veden erittymistä ja alentaa verenpainetta (kuva 11.20).
PNP:tä pidetään yleisesti fysiologisena angiotensiini II:n antagonistina, koska se aiheuttaa verisuonten laajenemista ja suolan ja veden menetystä.
AIHE 11.9. KALSIUM- JA FOSFAATTIAINEENAAN SÄÄTELY. PARATHORMONIN, KALSITRIOLIN JA KALSITONININ RAKENNE, SYNTEESI JA VAIKUTUSMEKANISMI
1. Aikuisen kehossa on -1,2 kg kalsiumia. Pääasiallinen kalsiumin rahasto kehossa on luun kalsium (99 % kaikesta kehon kalsiumista). Toinen rahasto on kalsiumionit liuotettuina nesteisiin tai yhdistettynä nesteiden ja kudosten proteiineihin. Kalsiumin pitoisuus solujen sisällä riippuu sen pitoisuudesta solunulkoisessa nesteessä. Ca 2 + -pitoisuus terveiden ihmisten veressä on 2,12-2,6 mmol / l (9-11 mg / dl), solunsisäisessä nesteessä - tuhat kertaa vähemmän.
Kalsium on luukudoksen tärkein mineraalirakennekomponentti. Kalsiumionit osallistuvat lihasten supistukseen, lisäävät solukalvon läpäisevyyttä kaliumioneille, vaikuttavat solujen natriuminjohtavuuteen, ionipumppujen toimintaan, edistävät hormonien eritystä, osallistuvat veren hyytymisen kaskadimekanismiin ja toimivat tärkeimmät välittäjät solunsisäisessä signaalinsiirrossa.
Plasman Ca 2 +:n pitoisuutta säädetään erittäin tarkasti: sen muutos vain 1 % aktivoi homeostaattisia mekanismeja, jotka palauttavat tasapainon. Tärkeimmät veren Ca 2+ -aineenvaihdunnan säätelijät ovat lisäkilpirauhashormoni, kalsitrioli ja kalsitoniini.
2. Parathormoni Lisäkilpirauhaset syntetisoivat sitä preprohormonina, joka sitten muunnetaan kypsäksi hormoniksi osittaisella proteolyysillä. PTH:ta erittyy vasteena veren kalsiumpitoisuuden laskulle. Hormonin pääkohdeelimet ovat luut ja munuaiset (kuva 11.21).
Hormoni käynnistää osteoblastien adenylaattisyklaasiin liittyvän tapahtumasarjan, joka stimuloi osteoklastien metabolista aktiivisuutta. Ca 2+:a mobilisoituu luusta ja fosfaatteja pääsee vereen, ja munuaisten distaalisissa tubuluksissa Ca 2+ -reabsorptio stimuloituu ja fosfaatin takaisinabsorptio vähenee, mikä johtaa normaalin kalsiumtason palautumiseen. ioneja solunulkoisessa nesteessä.
3. Kalsitrioli kuten muutkin steroidihormonit, se syntetisoituu kolesterolista. Kalsiferolin välitön esiaste on kolekalsiferoli (D3-vitamiini). Sisältää pienen määrän D3-vitamiinia
 Riisi. 11.21 PTH-toiminnan vaikutukset:
Riisi. 11.21 PTH-toiminnan vaikutukset:
1 - PTH stimuloi kalsiumin mobilisaatiota luusta; 2 - PTH stimuloi kalsiumionien uudelleenabsorptiota munuaisten distaalisissa tiehyissä; 3 - PTH aktivoi 1,25(OH) 2 D 3:n muodostumisen munuaisissa, mikä stimuloi Ca 2 +:n imeytymistä suolistossa
elintarvikkeissa, mutta suurin osa kalsitriolin synteesissä käytetystä vitamiinista muodostuu ihossa 7-dehydrokolesterolista ei-entsymaattisen reaktion aikana ultraviolettivalon vaikutuksesta. Kalsitriolin muodostuminen D 3 -vitamiinista alkaa maksassa ja päättyy munuaisiin (kuva 11.22).
Maksassa kolekalsiferoli hydroksyloituu 25. hiiliatomissa muodostaen 25-hydroksikolekalsiferolia. Munuaisissa 1o-hydroksylaasientsyymin vaikutuksesta tapahtuva hydroksylaatio on nopeutta rajoittava vaihe ja johtaa kalsitrioli 1,25(OH) 2 D 3 -muodostukseen - D 3 -vitamiinin aktiiviseen muotoon. Tämän reaktion entsyymi aktivoituu alhaisella Ca 2+ -ionipitoisuudella veressä ja lisäkilpirauhashormonilla. Kalsitriolin pitoisuuden nousu päinvastoin estää 1o-hydroksylaasin synteesiä munuaisissa, mikä estää hormonin muodostumista. Kalsitrioli kulkeutuu veren läpi kompleksissa kantajaproteiinin kanssa, ja se sitoutuu solunsisäiseen reseptoriin, on vuorovaikutuksessa kromatiinin kanssa ja muuttaa translaationopeutta. Tämän seurauksena kohdesoluissa syntetisoidaan proteiineja, jotka varmistavat kalsiumin ja fosfaattien imeytymisen enterosyytteihin.
4. Kalsitoniini - polypeptidi, joka koostuu 32 aminohappotähteestä, joissa on yksi disulfidisidos. Hormonia erittää parafollikulaarinen
 Riisi. 11.22 Kaavio kalsitriolin synteesiä varten:
Riisi. 11.22 Kaavio kalsitriolin synteesiä varten:
1 - kolesteroli on kalsitriolin esiaste; 2 - ihossa 7-dehydrokolesteroli muuttuu ei-entsymaattisesti kolekalsiferoliksi UV-säteilyn vaikutuksesta; 3 - maksassa 25-hydroksylaasi muuttaa kolekalsiferolin kalsidioliksi; 4 - munuaisissa kalsitriolin muodostumista katalysoi 1o-hydroksylaasi
Kilpirauhasen K-solut tai lisäkilpirauhasen C-solut korkean molekyylipainon prekursoriproteiinin muodossa. Kalsitoniinin eritys lisääntyy Ca 2 + -pitoisuuden kasvaessa ja vähenee, kun Ca 2 + -pitoisuus veressä laskee. Kalsitoniini estää Ca 2 +:n vapautumista luusta ja stimuloi sen erittymistä munuaisten kautta virtsaan.
5. hypokalsemia ja hyperkalsemia, kun kalsiumin pitoisuus veriplasmassa on normaalia pienempi tai korkeampi, viittaa patologiaan. Muutos veren kalsiumpitoisuudessa vaikuttaa kalsiumin pitoisuuteen solujen sisällä, mikä johtaa hermo- ja lihassolujen kiihtyvyyskynnyksen muutokseen, kalsiumpumpun toiminnan häiriintymiseen, entsyymiaktiivisuuden laskuun ja aineenvaihdunnan hormonaalisen säätelyn rikkominen. Hypokalsemialla havaitaan hyperrefleksejä, kouristuksia, kurkunpään kouristuksia. Hyperkalsemialla havaitaan hermo-lihashermoston vähenemistä, hermoston toiminnan syvää häiriötä, psykoosia, stuporia ja koomaa voi esiintyä.
6. Kilpirauhasen liikatoiminta. Lisäkilpirauhashormonin liiallinen eritys, joka johtuu lisäkilpirauhasen kasvaimesta, rauhasten diffuusista liikakasvusta, lisäkilpirauhasen karsinoomasta (primaarinen hyperparatyreoosi), johtaa lisääntyneeseen kalsiumin ja fosfaatin mobilisaatioon luusta, lisääntyneeseen kalsiumin takaisinimeytymiseen ja fosfaatin erittymiseen munuaisissa . Tämän seurauksena esiintyy hyperkalsemiaa, joka voi johtaa hermo-lihasherätyksen vähenemiseen ja lihasten hypotensioon. Potilaille kehittyy yleistä ja lihasheikkoutta, väsymystä ja kipua tietyissä lihasryhmissä, sekä selkärangan, reisiluun ja kyynärvarren luiden murtumien riski kasvaa. Fosfaatti- ja kalsiumionien pitoisuuden kasvu munuaistiehyissä voi aiheuttaa munuaiskivien muodostumista ja johtaa hyperfosfaturiaan ja hypofosfatemiaan.
7. Kilpirauhasen vajaatoiminta. Lisäkilpirauhasen vajaatoiminnasta johtuvan hypoparatyreoosin tärkein oire on hypokalsemia. Kalsiumionipitoisuuden lasku veressä voi aiheuttaa neurologisia, oftalmisia ja sydän- ja verisuonisairauksia sekä sidekudosvaurioita. Potilaalla, jolla on lisäkilpirauhasen vajaatoiminta, hermo-lihasjohtuminen lisääntyy, toonisia kouristuksia, hengityslihasten ja pallean kouristuksia ja kurkunpään kouristuksia.
8. Riisitauti- lapsuuden sairaus, joka liittyy luukudoksen riittämättömään mineralisaatioon. Luun mineralisaation häiriintyminen on seurausta kalsiumin puutteesta ja voi johtua seuraavista syistä: D 3 -vitamiinin puute ruokavaliossa, heikentynyt D 3 -vitamiinin imeytyminen ohutsuolessa, kalsitriolin esiasteiden synteesi heikkeneminen johtuen riittämättömästä ajasta aurinko, Ια-hydroksylaasin vika, kohdesolujen kalsitriolireseptorien vika. Kaikki tämä vähentää kalsiumin imeytymistä suolistossa ja sen pitoisuuden laskua veressä, stimuloi lisäkilpirauhashormonin eritystä ja sen seurauksena
Tämä on kalsiumionien mobilisointia luusta. Riisitauti vaikuttaa kallon luihin, rintakehä rintalastan kanssa työntyy eteenpäin, käsivarsien ja jalkojen putkimaiset luut ja nivelet ovat epämuodostuneet ja vatsa laajenee ja työntyy esiin. Pääasiallinen tapa estää riisitauti on oikea ravitsemus ja riittävä auringonpaiste.
TEHTÄVÄT OPIN ULKOPUOLISTA TYÖTÄ
Ratkaista ongelmia
1. Tutki vesitasapainon ylläpitämisen säätelymekanismeja, muista hormonien erittymistä aiheuttavat ärsykkeet ja niiden toimintamekanismin piirteet (kuva 11.19). Piirrä kaavio tapahtumasarjasta vesi-suolatasapainon palautumisessa suolaisen ruoan syömisen jälkeen.
2. 23-vuotiaalla miehellä aivolisäkkeen etuosan yläosasta kasvaneen poistamiseksi tehdyssä kirurgisessa leikkauksessa aivolisäkkeen takaosan kannas kärsii. Leikkauksen jälkeisenä aikana potilaalle kehittyi polyuria. Miten voit selittää tämän oireen ilmenemisen tällä potilaalla? Perustellaksesi vastauksesi:
a) nimeä hypotalamuksessa syntetisoidut ja aivolisäkkeen takaosasta erittyvät hormonit;
b) piirtää kaavio tämän hormonin signaalin välittymisestä kohdesoluihin;
c) Nimeä tämän hormonin vaikutukset.
3. Muista steroidihormonien synteesin kaavio (kuva 11.8) ja kirjoita muistikirjaan aldosteronin synteesin vaiheiden järjestys.
4. Piirrä oma kaavio, joka havainnollistaa aldosteronin vaikutuksia ja sen vaikutusmekanismia.
5. Tutki aldosteronin synteesin ja erittymisen säätelykaaviota reniini-angiotensiinijärjestelmän kanssa (kuva 11.19) ja valitse kaaviossa (Kuva 11.23) merkityt puuttuvat komponentit numeroin.
6. Tee oma kaavio, joka selittää PNF:n toiminnan päätulokset (kuva 11.20) ja vastaa kysymykseen, mikä on hypotensiivisen vaikutuksen perusta
7. Täytä taulukko. 11.3.
Taulukko 11.3. Vesi-suola-aineenvaihduntaa säätelevien hormonien ominaisuudet
 Riisi. 11.23. Vesi-suolan homeostaasin säätelykaavio
Riisi. 11.23. Vesi-suolan homeostaasin säätelykaavio
8. Täytä taulukko. 11.4.
Taulukko 11.4. Kalsium- ja fosfaattiaineenvaihduntaa säätelevien hormonien ominaisuudet
9. Käyttämällä kuvan kaaviota. 11.22, osoita kaikki mahdolliset riisitautien syyt ja esitä kaavio kalsitriolin signaalin välittymismekanismista kohdesoluihin.
10. Hypovitaminoosissa D 3 luun mineralisaatioprosessi häiriintyy, kalsiumin ja fosfaattien pitoisuus niissä vähenee; veren Ca 2 + -pitoisuus pysyy normaalialueella tai laskee hieman. Laadi kaavio Ca 2 + -homeostaasin ylläpitämiseksi hypovitaminoosissa D 3 ja määritä:
a) mistä lähteistä johtuen veren normaali Ca 2 + -pitoisuus säilyy tässä tapauksessa;
b) kuinka kalsitoniinin ja lisäkilpirauhashormonin pitoisuus veressä muuttuu.
11. Lisääntynyt kalsiumin erittyminen virtsaan voi olla syynä pääasiassa kalsiumoksalaatista koostuvien munuaiskivien muodostumiseen. Nimeä syyt, miksi Ca 2 -eritys voi lisääntyä.
ITSEHALLINTA TEHTÄVÄT
1. Valitse oikea vastaus.
Vasteena osmoottisen paineen nousuun hormonin synteesi ja eritys lisääntyvät:
A. Aldosteroni B. Kortisoli
B. Vasopressiini D. Adrenaliini D. Glukagoni
2. Aseta ottelu.
Synteesipaikka:
A. Maksa B. Munuaiset
B. Hypotalamus D. Lisämunuaiset
D. Haima
Metaboliitit:
1. Vasopressiini
2. Aldosteroni
3. Aseta ottelu:
A. Synteesin ja erityksen ärsyke on angiotensiini II:n muodostuminen B. Erityksen ärsyke on natrium-ionien pitoisuuden nousu
B. Kohde-elimet - ääreisvaltimot
D. Hormonin liikatuotanto johtaa polyuriaan D. Synteesipaikka - maksa
1. Vasopressiini
2. Aldosteroni
3. Angiotensinogeeni
4. Valitse oikeat vastaukset. Angiotensiini II:
A. Muodostunut maksassa
B. On proteolyyttinen entsyymi
B. On reniinin substraatti
D. Stimuloi aldosteronin synteesiä D. Stimuloi vasokonstriktiota
5. Valitse oikeat vastaukset.
Kalsitrioli:
A. Stimuloi kalsiumin reabsorptiota munuaisissa
B. On 7-dehydrokolesterolin esiaste
B. Stimuloi natriumin takaisinimeytymistä munuaisissa
D. Lisää kalsiumin imeytymistä suolistossa D. Stimuloi kalsiumin mobilisaatiota luista
6. Valitse oikeat vastaukset.
Ca 2 + -pitoisuuden lasku veriplasmassa aiheuttaa:
A. Lisäkilpirauhashormonin eritys
B. Kilpirauhasen parafollikulaaristen solujen toiminnan estäminen
B. D-vitamiinin metaboliittien hydroksylaatio 3 D. Kalsiumin erittymisen vähentäminen munuaisten kautta
D. Luun resorption nopeuden lisääminen
7. Suorita "ketju" -tehtävä:
a) Hypotalamuksen tuottama hormoni on:
A. Vasopressiini B. Adrenaliini
B. Aldosteroni G. Kalsitrioli
b) Tämän hormonin kohdesolut ovat:
A. JUGA solut
B. Ääreisvaltimot
B. Keräyskanavien ja distaalisten tubulusten solut D. Nefroniglomeruluksen solut
sisään) sitoutumalla näiden solujen reseptoreihin, se stimuloi:
A. Adenylaattisyklaasijärjestelmä B. Fosfoproteiinifosfataasi
B. Inositolitrifosfaattijärjestelmä D. Reniini-angiotensiinijärjestelmä.
G) tämän järjestelmän aktivoitumisen seurauksena proteiinin määrä kasvaa:
A. Albumiini
B. Natriumin kuljettajat
B. Aquaporina-2
G. Kaliumin kuljettaja
e) tämä proteiini lisää reabsorptiota:
A. Kaliumionit B. Kalsiumionit
B. Natriumionit D. Vesi
8. Valitse oikeat vastaukset. Parathormoni:
A. Se kuljetetaan veren läpi kompleksina kantajaproteiinin B kanssa. Eritystä säätelee veren kalsiumpitoisuus
B. Hormonipuutos johtaa keskittymiskyvyn laskuun
D. Biologisen aktiivisuuden ilmentymiseen tarvitaan koko hormonimolekyyli D. Lisää veden imeytymisen tehokkuutta suolistossa
9. Valitse oikeat vastaukset.
Vasopressiini:
A. Stimuloi veriplasman osmoottisen paineen nousua B. Aktivoi proteiinikinaasi C:tä munuaisissa
B. Stimuloi veden takaisinimeytymistä munuaisissa
D. Alentaa veriplasman osmoottista painetta D. Stimuloi akvaporiini-2-geenin ilmentymistä
10. Aseta ottelu:
A. Osoittaa verisuonia supistavaa vaikutusta B. Stimuloi Na+:n uudelleenabsorptiota
B. Vuorovaikuttaa kohdesolujen kalvoreseptorien kanssa D. Tehostaa reniinin eritystä
D. On proteolyyttinen entsyymi
1. Aldosteroni
2. Angiotensiini II
11. Valitse kaikki oikeat vastaukset. PNF:
A. Vuorovaikuttaa kohdesolujen kalvoreseptorien kanssa B. Aktivoi fosfolipaasi C:n
B. Aktivoi guanylaattisyklaasia
D. Estää aldosteronin erittymistä D. Lisää veden ja Na +:n erittymistä
12. Aseta ottelu:
A. Munuaisissa B. Ihossa
B. Maksassa D. Aivoissa
D. Suolistossa
1. 7-dehydrokolesterolin muuntaminen D 3 -vitamiiniksi ei-entsymaattisella fotolyysillä
2. 1,25 (OH)2D 3:n muodostuminen mono-oksigenaasireaktiossa, jossa on mukana NADPH
3. Kalsiumia sitovan proteiinisynteesin induktio VASTAUKSIEN STANDARDIT "ITSEENHALLINTA TEHTÄVÄT"
1. AT 7. a) A, b) C, c) A, d) C, e) D
2. 1-B; 2-G; 3-B 8. B, C
3. 1-B; 2-A; 3-D 9. C, D, D
4. G, D 10. 1-B; 2-A; 3-D
5. A, G, D 11. A, C, D, D
6. A, C, D, D 12 .1 - B; 2 - B; 3 - D
PERUSKÄSITTEET JA KÄSITTEET
1. Vesi-suolan homeostaasi
2. Diabetes insipidus
3. Reniini-angiotensiini-aldosteronijärjestelmä
4. Hyperaldosteronismi
5. Hyperkalsemia
6. Hypokalsemia
7. Kilpirauhasen vajaatoiminta
8. Kilpirauhasen liikatoiminta
TEHTÄVÄT KUULUTUSTYÖHÄN
Ratkaista ongelmia
1. Jotkut verenpainetaudin muodot johtuvat erilaisista munuaishäiriöistä, kuten kasvaimen aiheuttamasta munuaisvaltimon puristumisesta. Pääasiallinen hoitomenetelmä tällaisissa tapauksissa on vahingoittuneen elimen (munuaisen) poistaminen. Potilaiden tilan paraneminen kuitenkin havaitaan, kun potilaille määrätään ACE:n estäjiä. Piirrä kaavio, joka näyttää muutoksen vesi-suola-aineenvaihdunnassa munuaisvaltimon puristuksen aikana. Minkä muutosten seurauksena potilaan tila paranee?
2. Lääkäriin tuli potilas, joka valitti usein virtsaamisesta ja jatkuvasta janon tunteesta. Tutkimuksessa havaittiin virtsan päivittäisen määrän lisääntyminen ja sen tiheyden jyrkkä lasku. Analyysi osoitti, että insuliinitaso oli normaalin rajoissa, mutta veden takaisinimeytymisestä vastaavan hormonin pitoisuudessa havaittiin nousu. Mikä on polyurian syy tällä potilaalla? Vastataksesi kysymykseen:
a) nimeä tämä hormoni;
b) luettele ärsykkeet, jotka aiheuttavat sen erittymisen;
c) nimeä tämän hormonin reseptorityypit ja niiden sijainnit;
d) antaa kaavio tämän hormonin signaalinsiirrosta munuaisissa;
e) kuvaa hormonin vaikutuksia kohdekudoksiin;
f) Esitä kaavio tämän hormonin erityksen säätelystä.
3. 48-vuotias mies kääntyi lääkärin puoleen valittaessaan heikkoutta, lihaskipua, ummetusta sekä viimeaikaisia selkä- ja virtsankipukohtauksia. Tutkimuksen aikana potilaalla todettiin primaarinen lisäkilpirauhasen liikatoiminta, joka oli seurausta lisäkilpirauhasen vasemman lohkon hyvänlaatuisen hypersekretorisen kasvaimen kehittymisestä.
Selitä, miksi munuaiskivitauti voi kehittyä hyperparatyreoosissa? Käytä tehtävän ratkaisussa tehtävän 5 kaavioita.
4. Nainen kääntyi lastenlääkärin puoleen valittaen, että hänen kaksivuotiaasta pojastaan oli tullut oikukas, ärtyisä ja huonosti syönyt. Hikoilu ilmaantui, uloste oli epävakaa. Tutkimuksessa todettiin kallon luiden yhteensopivuus, rintakehän epämuodostuma. Biokemiallisessa verikokeessa kokonaiskalsiumin taso on 1,57 mmol / l (normi on 2,3-2,8 mmol / l). Arvaa, mistä sairaudesta tämä lapsi kärsii. Tätä varten:
a) vertaa lapsen veren kokonaiskalsiumin määrää normiin, anna tälle tilalle nimi;
b) ilmoittaa mahdolliset syyt, jotka voivat johtaa tämän taudin kehittymiseen;
c) antaa kalsiumin aineenvaihdunnan hormonaalisen säätelyn synteesikaavion;
d) ilmoittaa hormonien toimintamekanismit, niiden puutteen syyt ja seuraukset kehossa;
5. Tutki kaaviota:
Kilpirauhasen vajaatoiminnan syyt ja seuraukset (kuva 11.24). Tee samanlaisia kaavioita:
a) hyperparatyreoosi;
b) riisitauti
 Riisi. 11.24. Hypoparatyreoosin syyt ja seuraukset
Riisi. 11.24. Hypoparatyreoosin syyt ja seuraukset
|
esittely Erillinen ruoka I.1 Erillisillä aterioilla on historiaa I.2 Jonkin asian täydellinen hylkääminen ei tule kysymykseen I.4 Erilliset ateriat, koska se on järkevää I.6 Tasapaino on avainasemassa I.9 Tärkeimmät kasvituotteemme I.14 Ulkona ruokailevien ongelmat I.14 Ruoansulatuksen vuorokausirytmit ruoka ja sairaudet II.1 Ravitsemus, ruumiinpaino ja hormonaalinen tila II.3 Migreeni ja ravitsemus II.4 Elintarvikkeet ja tartuntataudit II.5 Rasvat, stressi ja ravitsemus II.6 Makea ruoka - katkera kosto Johtopäätös Bibliografia Sovellukset Liite 1. Aikuisen keskimääräinen päivittäinen tasapainoinen ravintoaineiden ja energian tarve (A. A. Pokrovskyn tasapainoinen ravitsemuskaava) |
JOHDANTO
Venäjällä on alhainen ravitsemustietokulttuuri. Ne perustuvat perinteisiin lähestymistapoihin ottamatta huomioon kulutettujen tuotteiden koostumuksen muutoksia, ne eivät ole samaa mieltä ja ovat usein ristiriidassa ihmisen fysiologian tietämyksen kanssa.
Joten mitä tapahtuu perinteiselle ruokavaliollemme? Mahaan joutuva voipuuro (rasvatärkkelys) tai maitopuuro (proteiinitärkkelys) muuttuu happamien ja emäksisten ympäristöjen seokseksi, jotka neutraloivat toisiaan. Neutraalissa ympäristössä ravintoaineet eivät hajoa, vaan mahalaukussa elävät putrefaktiiviset bakteerit käsittelevät niitä. Seurauksena on, että sinne muodostuu mätänevä "roskakaatos". Päästäkseen eroon siitä keho pakotetaan mobilisoimaan puolustuskykynsä, tuottamaan suuren määrän leukosyyttejä, mikä kuluttaa lisäenergiaa, joten jos perinteisen aamiaisen jälkeen haluat pian syödä, keho (sen solut) pysyi nälkäisenä. , ja käytti voimansa neutraloimaan "roskaa" (elintarvikkeiden leukosytoosi).
Perinteinen lounas - keitto lihaliemellä - rasvat + tärkkelys + proteiinit. Jälleen selviää kylläisyyteen sekoitettu vatsan ylivuoto.
Ihmiskeholla on erittäin suuri turvamarginaali. Tieteelliset laskelmat osoittavat, että elinikä voi olla 400 vuotta. Nuoret syövät kaikkea ja sanovat, että kaikki on kunnossa. Mutta jo 30-35 vuoden kuluttua ihminen alkaa hankkia "kimpun sairauksia". Aamulla ei ole iloisuutta, iltapäivällä - uneliaisuutta, illalla - väsymystä - tästä tulee kypsän ihmisen normaali tila. Sen ei pitäisi olla niin. Sairaiden lasten syntymä (terveitä lapsia ei synny melkein koskaan) osoittaa, että ihmiskunnan turvallisuusmarginaali on ehtynyt. Luonnonvalinta on alkanut. Terveyden määrä vähenee sukupolven myötä. Jos otamme isoisiemme terveyden 100 %:ksi, niin isillä on 50 %, meidän sukupolvellamme - lapsella - 25 %, seuraava sukupolvi on kaikki sairaana hedelmöityshetkestä lähtien. Selviytymisen takaavat vain lääkitys, ennaltaehkäisevät toimenpiteet, oikea ravitsemus ja terveellisten elämäntapojen noudattaminen.
Erillinen ruoka
Kiitos
Sivusto tarjoaa viitetietoja vain tiedoksi. Sairauksien diagnosointi ja hoito tulee suorittaa asiantuntijan valvonnassa. Kaikilla lääkkeillä on vasta-aiheita. Asiantuntijan neuvoja kaivataan!
Mikä on hormonaalinen epätasapaino?
Ihmiskehon endokriiniset rauhaset tuottavat noin 70 hormonit. Näiden hormonien normaali suhde toisiinsa varmistaa terveen organismin elintärkeiden prosessien vakauden. Mutta kannattaa lisätä tai vähentää ainakin yhden hormonin tuotantoa, kuten hormonaalinen häiriö(epäonnistuminen). Erityisen usein naisilla on hormonaalinen epäonnistuminen, joka rikkoo naissukupuolihormonien synteesiä.Naisen kehon hormonaalisen epäonnistumisen merkit voivat olla erilaisia: ensinnäkin tämä on kuukautiskierron rikkomus. Lisäksi naisten hormonaaliset häiriöt voivat ilmetä:
- liiallinen tai riittämätön hiusten kasvu;
- maitorauhasten alikehittyneisyys;
- äkillinen painonnousu;
- hermostuneisuus, ärtyneisyys tai masennus;
- liiallinen hikoilu;
- päänsärkyä ja monia muita oireita.
Naisten hormonaalisen epätasapainon syyt
Naisen herkkää hormonaalista tasapainoa voivat häiritä useat tekijät:- huonot tavat (tupakointi, alkoholin väärinkäyttö);
- irrationaalinen ravitsemus;
- krooninen unenpuute;
- istuva elämäntapa tai päinvastoin liiallinen fyysinen aktiivisuus;
- hormonaalisten ehkäisyvälineiden toistuva käyttö;
- toistuvat abortit;
- siirretyt infektiot (ARVI, tonsilliitti, tippuri, klamydia, kuppa jne.).
Menetelmät hormonaalisten häiriöiden hoitoon
Tietenkin ensinnäkin hormonaalisia häiriöitä hoidetaan hormonaalisilla lääkkeillä. Mutta useimmissa tapauksissa hormonaalinen tausta voidaan palauttaa muiden kuin lääkkeiden hoitomenetelmien avulla, joihin kuuluvat:- terveellinen elämäntapa (riittävä uni, liikkuminen raikkaassa ilmassa, aamuharjoitukset, huonojen tapojen hylkääminen);
- oikea ravitsemus (ruokavalio, jossa on valtaosa kasvituotteista ja kasvirasvoista);
- Fysioterapiaharjoitukset;
- fysioterapia, mukaan lukien hieronta;
- balneoterapia (kylvyt erilaisilla kivennäisvesillä);
- Kylpylähoito.
Ravitsemus hormonaalisen epäonnistumisen varalta
 Jos hormonaalinen tila rikkoutuu, naisten on muutettava päivittäistä ruokavaliotaan sisällyttämällä mahdollisimman paljon kasvisruokaa - vihanneksia, hedelmiä, marjoja, sieniä. Tosiasia on, että nämä tuotteet sisältävät fytoestrogeenejä - aineita, joilla on samanlaiset ominaisuudet kuin naissukupuolihormonien ominaisuudet.
Jos hormonaalinen tila rikkoutuu, naisten on muutettava päivittäistä ruokavaliotaan sisällyttämällä mahdollisimman paljon kasvisruokaa - vihanneksia, hedelmiä, marjoja, sieniä. Tosiasia on, että nämä tuotteet sisältävät fytoestrogeenejä - aineita, joilla on samanlaiset ominaisuudet kuin naissukupuolihormonien ominaisuudet. Fytoestrogeenejä löytyy palkokasveista (herneistä, papuista), vehnän jyvistä ja alkioista sekä sipulista. Niitä löytyy myös munista (kana, viiriäinen jne.). Esimerkiksi munakas, jossa on sipulia ja sieniä, on tyypillinen "naisellinen" ruokalaji, joka sisältää huomattavan määrän kasviestrogeenejä.
Naisten hormonaalisten häiriöiden yhteydessä tarvitaan sinkkiä ja seleeniä sisältäviä tuotteita kehon omien hormonien tuotannon normalisoimiseksi. Tällaisia ruokia ovat vähärasvainen liha (naudanliha), laardi, kaurapuuro, maito, kaikki lehtivihannekset (salaatti, kaali, tilli, persilja, pinaatti, basilika, vesikrassi jne.), pähkinät (maapähkinät, mantelit, pistaasipähkinät), kurpitsansiemenet, valkosipuli .
On suositeltavaa jättää ruokavaliosta pois (tai rajoittaa minimiin) sellaiset elintarvikkeet kuten sokeri, hunaja, leivonnaiset, makeiset, suklaa, kondensoitu maito, perunat, liha (sianliha, hanhi, ankka), säilykkeet, makkarat, makkarat.
Jos hormonaalinen epäonnistuminen on johtanut voimakkaaseen painonnousuun, painonpudotus saavutetaan hormonaalisen (aineenvaihdunnan) ruokavalion avulla.
Hormonaalinen ruokavalio
Tämä ruokavalio aktivoi rasvanpolttoa edistävien hormonien synteesin (testosteroni, adrenaliini, norepinefriini) ja estää sellaisten hormonien tuotantoa, jotka aiheuttavat rasvan kertymistä elimistöön (insuliini, estrogeeni).Hormonaalisen ruokavalion vaiheet:
1.
Nopea ja aktiivinen rasvanpoltto (noin 2 viikkoa).
2.
Vakaa rasvanpoltto (määräämätön kesto).
3.
Painon pitäminen saavutetulla alhaisella tasolla.
Päivittäisen ruokalistan laatimisen helpottamiseksi hormonaalisen ruokavalion eri vaiheissa kaikki ruoat on jaettu viiteen ryhmään, joilla on eri arvosanat. Mitä korkeampi pistemäärä, sitä voimakkaampi rasvakertymä tätä tuotetta käytettäessä. Ja päinvastoin: "0 pistettä" -ryhmään määritetyt tuotteet eivät edistä rasvojen laskeutumista, vaan niiden polttamista.
| Pisteet | Ruoka |
| 0 | Munat, kala, katkaravut, kalmari, simpukat, kani, kana (valkoinen liha rinnasta), kalkkuna (valkoinen liha rinnasta), sienet, vihannekset, lime, sitruuna, tilli, persilja, sinappi, piparjuuri, vihreät herneet, maitotuotteet tuotteet, joiden rasvapitoisuus on enintään 2 %. |
| 1 | Marjat, pavut, vastapuristetut vihannesmehut. |
| 2 | Kana, naudanliha, vasikanliha, kasviöljyt, pähkinät (saksanpähkinät, hasselpähkinät, pistaasipähkinät), leipä leseillä, keitetyt porkkanat ja punajuuret, hedelmät, oliivit, oliivit, fetajuusto, fetajuusto, ruskea riisi, kaurapuuro, tattari, rasvaton meijeri tuotteita yli 4 %. |
| 3 | Kaikki juustot, hirssi, jogurtti lisäaineilla, tumma suklaa, mysli, vastapuristetut hedelmämehut. |
| 4 | Sianliha, ankka, hanhi, makkara, makkarat, perunat, sokeri, hunaja, kuivatut hedelmät, muffinit, maitosuklaa, makeiset, jäätelö, mannasuurimot, öljysäilykkeet, yli 4% rasvapitoiset maitotuotteet. |
Noudattamalla hormonaalista ruokavaliota sinun on noudatettava seuraavia sääntöjä sen jokaisessa vaiheessa:
1.
Voit syödä kerralla enintään 250-300 ml ruokaa (tilavuus on hieman yli 1 lasi), olipa kyseessä lounas, aamiainen tai päivällinen.
2.
Aterioiden välillä ei saa olla yli kolmea tuntia.
3.
Muista juoda 2 (tai enemmän) litraa vettä päivässä.
Ruokailuohjelma on suunnilleen seuraava:
- Aamiainen - viimeistään klo 10.00;
- 2. aamiainen - viimeistään klo 12.00;
- Lounas - viimeistään klo 15.00;
- Iltapäivän välipala - viimeistään klo 18.00;
- Illallinen - viimeistään klo 20.00.
Ravitsemus hormonaalisen ruokavalion 1. vaiheessa täytyy olla hyvin niukka. Vain 0 pistettä sisältäviä ruokia saa syödä. Oliiviöljyä sallitaan 1 ruokalusikallinen päivässä.
Samaan aikaan paino laskee nopeasti, joten sinun on seurattava hyvinvointiasi huolellisesti. Äkillinen heikkous, silmien tummuminen, tinnitus - sinun tulee juoda välittömästi vahvaa makeaa teetä ja makaamaan. Tällaiset oireet ovat merkki siitä, että sinun on siirryttävä hormonaalisen ruokavalion toiseen vaiheeseen. Joka tapauksessa ensimmäisen vaiheen kesto on enintään kaksi viikkoa.
Ravitsemus hormonaalisen ruokavalion 2. vaiheessa tapahtuu seuraavasti:
- Aamiainen - 4 pistettä;
- 2. aamiainen - 2 pistettä;
- Lounas - 2 pistettä;
- Iltapäivän välipala - 1 piste;
- Illallinen - 0 pistettä.
Valitse esimerkiksi 1 tuote 3 pisteen luettelosta + 1 tuote 1 pisteen luettelosta + mikä tahansa määrä 0 pisteen tuotteita (älä unohda rajoitettua kokonaismäärää!).
Tai: 1 tuote 4 pistettä + useita 0 pisteen tuotteita.
Tai: 2 tuotetta 2 pisteen listalta.
Valitse samalla tavalla ruoka-aineet jokaiselle aterialle. Pisteiden kokonaismäärä voi olla suositeltua pienempi, mutta ei missään tapauksessa enempää. Jos yksi ateria jätetään väliin, sen pisteitä ei lisätä seuraavaan ateriaan.
Hormonaalisen ruokavalion 2. vaiheella ei ole kestorajoituksia. Paino laskee asteittain ja tasaisesti. Kun saavutat halutun tuloksen, siirry kolmanteen vaiheeseen.
Ravitsemus hormonaalisen ruokavalion 3. vaiheessa suoritetaan seuraavasti: valitse yksi ateria (esimerkiksi lounas) ja lisää siihen 1 piste. Hallitse painoasi. Jos laihtuminen jatkuu, voit lisätä 1 pisteen toiseen ateriaan. Pisteiden lisääminen jatkuu, kunnes painonpudotus pysähtyy.
hCG hormonaalinen ruokavalio
 Laihtumiseen on toinenkin ruokavalio, jota kutsutaan myös hormonaaliseksi, mutta sen käytön tulokset ovat erittäin kyseenalaisia. Tämä ruokavalio koostuu siitä, että ruokavaliossa käytetään vain vähäkalorisia ruokia, ja nainen saa samanaikaisesti hCG-hormonin (ihmisen koriongonadotropiinin) injektioita. Normaalisti tämä hormoni syntetisoituu naisen kehossa raskauden aikana.
Laihtumiseen on toinenkin ruokavalio, jota kutsutaan myös hormonaaliseksi, mutta sen käytön tulokset ovat erittäin kyseenalaisia. Tämä ruokavalio koostuu siitä, että ruokavaliossa käytetään vain vähäkalorisia ruokia, ja nainen saa samanaikaisesti hCG-hormonin (ihmisen koriongonadotropiinin) injektioita. Normaalisti tämä hormoni syntetisoituu naisen kehossa raskauden aikana. Tämän ruokavalion tehokkuudesta ei ole vakuuttavia todisteita, ja hCG-hormonin käyttöönotto voi johtaa arvaamattomiin tuloksiin. On suuri todennäköisyys kehittää vieläkin vakavampia hormonaalisia häiriöitä. Siksi tieteellinen lääketiede vastustaa ehdottomasti tämän ruokavalion käyttöä.
Fytoterapia hormonaalisten häiriöiden hoitoon
Lääkeyrtit voivat auttaa korjaamaan hormonaalista epätasapainoa. Kansanlääketieteessä tähän tarkoitukseen käytetään seuraavien kasvien infuusioita ja tinktuuroita:- alalla neilikka;
- oregano ("naarasruoho");
- keuhkojuuri;
- hanhen cinquefoil;
- toukokuu nokkonen;
- lehmus kukat;
- pellavansiemeniä jne.
Infuusiot valmistetaan useimmiten vakiojärjestelmän mukaan (rkl yrttejä lasilliseen kiehuvaa vettä, vaadi kunnes jäähtyy). Tällä tavalla haudutettua peltokynän infuusiota naisten hormonaalisten häiriöiden hoitoon suositellaan juotavaksi kahden viikon ajan 4 kertaa päivässä, 1/4 kuppia.
Kun hormonaalinen epätasapaino ilmenee, kehittyy usein amenorrea (kuukautisten puuttuminen). Tässä tapauksessa perinteinen lääketiede suosittelee sipulien tai niiden kuorien käyttöä:
- Lasillinen sipulinkuorta kaadetaan 0,5 litraan kiehuvaa vettä, keitetään 20 minuuttia, annetaan jäähtyä, suodatetaan ja otetaan kolme kertaa päivässä ruokalusikalliseen (ennen ateriaa).
- Ota 5 päätä keskikokoista sipulia ja 3-4 valkosipulinkynttä. Puhdistetaan, murskataan ja kaadetaan kolmella lasillisella maitoa. Kuumenna miedolla lämmöllä sipulin ja valkosipulin seos pehmeäksi. Sen jälkeen ne poistetaan lämmöltä, annetaan jäähtyä hieman ja sekoitetaan kolmeen teelusikalliseen hunajaa. Seos otetaan 3 kertaa päivässä ruokalusikallista, kunnes lääke loppuu (sinun on säilytettävä jääkaapissa).
Fysioterapia hormonaaliseen epätasapainoon
 Fysioterapiamenetelmiä käytetään usein naisten hormonaalisten häiriöiden hoidossa. Nämä menetelmät ilman lääkealtistusta antavat sinun säätää häiriintynyttä kuukautiskiertoa, parantaa munasarjojen toimintahäiriötä, amenorreaa ja muita hormonaaliseen epäonnistumiseen liittyviä patologisia prosesseja naisen kehossa. Lisäksi fysioterapeuttiset hoitomenetelmät lisäävät vastustuskykyä ja kehon yleistä vastustuskykyä haitallisia ympäristötekijöitä vastaan.
Fysioterapiamenetelmiä käytetään usein naisten hormonaalisten häiriöiden hoidossa. Nämä menetelmät ilman lääkealtistusta antavat sinun säätää häiriintynyttä kuukautiskiertoa, parantaa munasarjojen toimintahäiriötä, amenorreaa ja muita hormonaaliseen epäonnistumiseen liittyviä patologisia prosesseja naisen kehossa. Lisäksi fysioterapeuttiset hoitomenetelmät lisäävät vastustuskykyä ja kehon yleistä vastustuskykyä haitallisia ympäristötekijöitä vastaan. Naisten hormonaalisten toimintahäiriöiden yhteydessä seuraavat fysioterapiamenetelmät ovat tehokkaimpia:
- kohdunkaulan sähköstimulaatio;
- akupunktio;
- laserhoito (mukaan lukien ILBI);
- kaulusalueen elektroforeesi novokaiinilla;
- aivojen galvanointi;
- hieronta (yleinen ja gynekologinen);
- hirudoterapia (hoito iilimatoilla).
Hoito iilimatoilla - hirudoterapia - on tehokas kaikissa hormonaalisissa patologioissa, mukaan lukien naisten hormonaaliset epäonnistumiset. Iilimatojen sylki sisältää aineita, jotka stimuloivat elimistöstä puuttuvien hormonien tuotantoa. Hormonitasapainon korjaamiseksi iilimatoja asetetaan yleensä sacrococcygeal alueelle. Iilimatojen sijoittaminen tälle alueelle ei vain palauta häiriintynyttä hormonaalista tasapainoa, vaan myös stimuloi kehon puhdistamista myrkkyistä.
Naisten hormonaalisten toimintahäiriöiden laserhoitoa käytetään altistumisena sisäelimille (vatsan seinämän tai emättimen kautta) ja ILBI:n muodossa - suonensisäisenä laserveren säteilytyksenä.
Lasersäteen vaikutus sisäelimiin on täysin kivutonta, sillä ei ole sivuvaikutuksia ja se antaa pitkäaikaisen vaikutuksen hoidosta.
ILBI on yleinen hoitomenetelmä, turvallinen ja erittäin tehokas. Laskimonsisäinen veren säteilytys matalataajuisella laserilla vaikuttaa hellävaraisesti kehoon stimuloiden itsesäätelyjärjestelmää ja korjaamalla hormonaalisia häiriöitä. ILBI:tä voidaan käyttää yksinään tai osana monimutkaista hoitoa.
Psyykkisen tilan korjaaminen hormonaalisissa häiriöissä
 Joissakin tapauksissa hormonaalisten vajaatoimintapotilaiden henkinen tila kärsii niin paljon, että se vaatii erityistä korjausta. Erityisen usein havaitaan psykoemotionaalisia häiriöitä
Joissakin tapauksissa hormonaalisten vajaatoimintapotilaiden henkinen tila kärsii niin paljon, että se vaatii erityistä korjausta. Erityisen usein havaitaan psykoemotionaalisia häiriöitä


